一 : 凯美纳说明书
通用名称:
盐酸埃克替尼片
功能主治:
本品单药适用于治疗既往接受过至少一个化疗方案失败后的局部晚期或转移性非小细胞肺癌(NSCLC),既往化疗主要是指以铂类为基础的联合化疗。(www.61k.com]该适应症主要基于一项随机、对照、双盲研究中显示出盐酸埃克替尼(以下简称埃克替尼)对于这类患者无进展生存期的疗效不劣于吉非替尼,进一步的总生存数据尚在收集中。
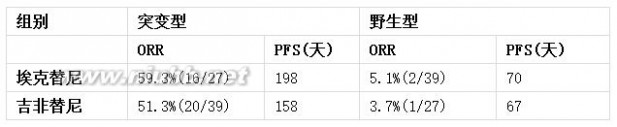
该研究中获得表皮生长因子受体(EGFR)突变检测结果的亚组人群初步分析结果显示,EGFR突变型患者疗效优于野生型患者,但对于EGFR突变型或野生型亚组人群的作用差别尚需进一步大样本研究证实(见【临床试验】)。
对于不同病理类型的亚组人群分析结果初步提示,非鳞癌患者疗效优于鳞癌患者。同样,对于鳞癌和非鳞癌亚组人群的作用差别尚需进一步大样本研究证实(见【临床试验】)。
建议经治医生结合同类药物相关研究结果及患者自身状况综合考虑适宜的治疗选择。
用法用量:
本品的推荐剂量为每次125mg(1片),每天三次。口服,空腹或与食物同服,高热量食物可能明显增加药物的吸收(见【药代动力学】)。
剂量调整:当患者出现不能耐受的皮疹、腹泻等不良反应时,可暂停(1~2周)用药直至症状缓解或消失;随后恢复每次125mg(1片),每天三次的剂量;对氨基转移酶轻度升高[丙氨酸氨基转移酶(ALT)及天门冬氨酸氨基转移酶(AST)低于100 IU/L]的患者可继续服药但应密切监测;对氨基转移酶升高比较明显(ALT及AST在100 IU/L以上)的患者,可暂停给药并密切监测氨基转移酶,当氨基转移酶恢复(ALT及AST均低于100 IU/L,或正常)后可恢复给药(见【不良反应】)。
目前尚无针对特殊人群包括老年、儿童、孕妇或肝、肾功能不全患者的临床研究结果。
对在不同年龄和性别等患者血药浓度资料分析结果显示患者的血药浓度不受年龄和性别等因素的影响(见【老年用药】),故不推荐根据年龄和性别调整剂量。
剂型:
片剂
不良反应:
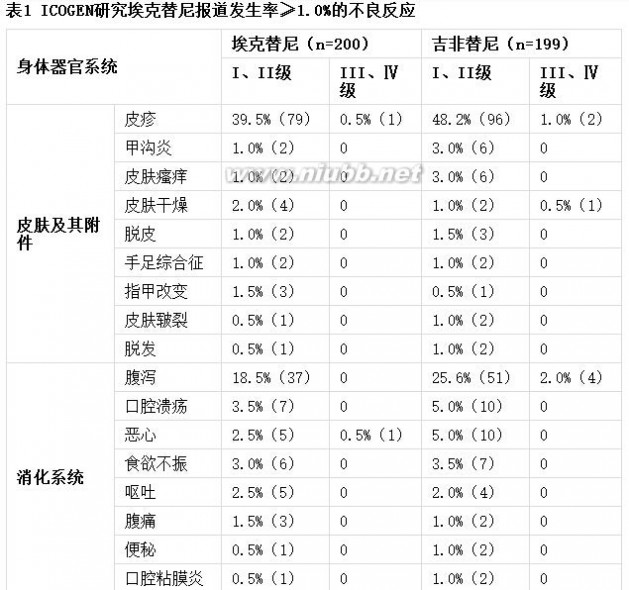
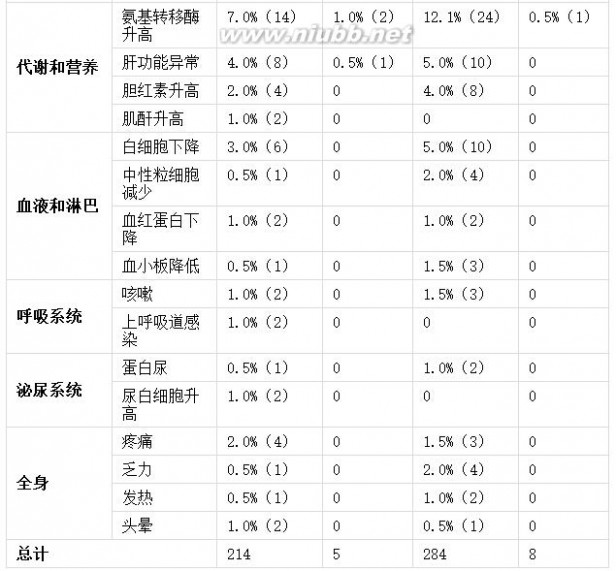
埃克替尼的安全性评估是基于 312例晚期NSCLC患者的研究数据,包括224例接受125mg每天三次剂量的治疗。总体上埃克替尼耐受性良好。III期临床试验(ICOGEN)最常见不良反应为皮疹(39.5%)、腹泻(18.5%)和氨基转移酶升高(8.0%),绝大多数为I~II级,一般见于服药后1-3周内,通常是可逆性的,无需特殊处理,可自行消失。表1列出了在ICOGEN试验中报道的发生率≥1%的不良反应。
禁忌:
已知对该活性物质或该产品任一赋形剂有严重过敏反应者。
注意事项:
?1、据文献报道,接受吉非替尼和厄洛替尼治疗的东方人群间质性肺病(ILD)发生率分别为2-3%和1-2%。在ICOGEN临床研究中未观察到发生间质性肺病。间质性肺病患者通常出现急性呼吸困难,伴有咳嗽、低热、呼吸道不适和动脉血氧不饱和等。短期内该症状可发展得很严重,并致患者死亡。放射学检查常显示肺浸润或间质有毛玻璃样阴影。
经治医生治疗期间应密切监测间质性肺病发生的迹象,如果患者出现新的急性发作或进行性加重的呼吸困难、咳嗽,应中断本品治疗,立即进行相关检查。当证实有间质性肺病时,应停止用药,并对患者进行相应的治疗。
文献报道,出现间质性肺病的高风险因素包括:吸烟、较差的体力状态(PS≥2)、在CT扫描上正常肺组织覆盖范围≤50%、距非小细胞肺癌诊断时间较短(<6个月)、原有间质性肺炎、年龄较大(≥ 55岁)、伴有心脏疾病。存在上述高风险因素的患者使用本品治疗时应谨慎。
2.已观察到少数患者一过性肝氨基转移酶升高(见【不良反应】)。因此,建议定期检查肝功能,特别是在用药的前一个月内。肝脏氨基转移酶轻度升高的患者应慎用本品。氨基转移酶中度升高或以上的患者需暂停用药,监测氨基转移酶直至其升高缓解或消失可恢复用药(见【用法用量】)。
3.如以下情况加重,应即刻就医:新的急性发作或进行性加重的呼吸困难、咳嗽;严重或持续的腹泻、恶心、呕吐或厌食。
4.对驾驶及操纵机器能力的影响:在本品治疗期间,可出现乏力的症状,出现这些症状的患者在驾驶或操纵机器时应给予提醒。
成份:
【化学名称】 ?4-[(3-乙炔基苯基)氨基]-喹唑啉并[6,7-b]-12-冠-4 盐酸盐。
性状:
本品为棕红色薄膜衣片,去除包衣后显类白色。
孕妇及哺乳期妇女用药:
1.目前尚无本品用于妊娠期女性的临床资料。动物实验结果表明,在器官发生期给予可对母体产生毒性的高剂量埃克替尼,在大鼠中可观察到死胎率升高,部分胎鼠颈背部或眼周淤血。在大鼠中未观察到外观、内脏畸形及骨化率异常。
建议育龄女性在接受本品治疗期间避免妊娠。
2.哺乳期使用:目前尚无本品用于哺乳期女性的临床资料。尚不清楚埃克替尼或其代谢产物是否会分泌入人乳中。
建议哺乳母亲在接受本品治疗期间停止母乳喂养。
儿童用药:
目前尚无本品用于18岁以下儿童或青少年患者安全性与疗效的资料,故不推荐使用。
老年用药:
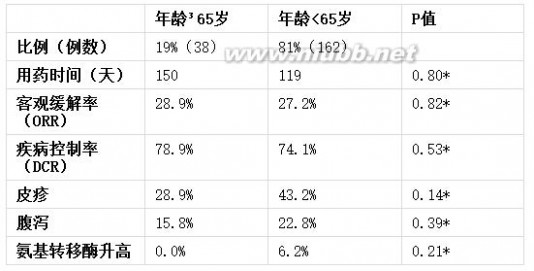
目前尚无特殊针对老年患者的临床研究资料。在ICOGEN研究中受试者年龄65岁以上患者占19.0%。与65岁以下受试者相比, 65岁以上患者的平均用药时间(天数)略高于65岁以下组, 皮疹、腹泻和氨基转移酶升高的发生率略低于后者,疗效相近(详见表2)。年龄似乎并非埃克替尼的用药剂量、疗效和安全性的影响因素。因65岁以上患者比例有限,故尚不能获得肯定结论。
表2 年龄在65岁以上与65岁以下的受试者用药剂量、疗效及安全性比较
药物相互作用:
目前埃克替尼尚未进行正式的药物相互作用研究。体外试验表明,埃克替尼主要通过细胞色素P-450单加氧酶系统的CYP2C19和CYP3A4代谢,对CYP2C9和CYP3A4有明显的抑制作用,未发现对大鼠肝P450酶有明显诱导作用。
因此,在与下列药物合用时应注意潜在的药物相互作用:CYP2C19诱导剂(如氨鲁米特)和CYP3A4诱导剂(如奈夫西林、奈韦拉平、苯巴比妥和利福霉素类);CYP2C9底物(如华法林)和CYP3A4底物(如苯二氮卓类、钙通道阻断剂、那格列奈、麦角碱衍生物等)。
药理作用:
药理作用
埃克替尼是一种选择性表皮生长因子受体(EGFR)酪氨酸激酶抑制剂。埃克替尼抑制EGFR酪氨酸激酶活性的半数有效浓度(IC50)为5nM,在所测试的88种激酶中,500nM浓度的埃克替尼只对EGFR野生型及其突变型有明显的抑制作用,对其它激酶均没有抑制作用,提示埃克替尼是一个高选择性的EGFR激酶抑制剂。体外研究和动物实验表明埃克替尼可抑制多种人肿瘤细胞株的增殖。
毒理研究
临床前研究资料表明,埃克替尼安全性良好,仅在犬连续多次给药270天时,在60mg/kg给药剂量组见氨基转移酶偏高等可逆性毒性反应。
在基因突变分析(细菌和体外哺乳动物细胞)、体外哺乳动物细胞和体内小鼠微核试验中,埃克替尼未显示遗传毒性作用。埃克替尼对雄性小鼠生殖功能及生殖系统无明显影响,对Wistar大鼠无致畸胎作用。埃克替尼对孕鼠生殖功能及胚胎生长发育有抑制作用。在高剂量(300mg/kg)时,可使活胎率和胎重显著下降,部分胎鼠颈背部或眼周淤血,但未见外观、内脏畸形及骨化率异常。
目前尚未开展致癌性研究。
药物过量:
目前尚不清楚过量服用埃克替尼可能产生的症状,也没有针对服用过量埃克替尼的特异治疗方法。在I期临床试验中,部份患者服用剂量达400mg,每日三次 时,不良反应(主要是皮疹和腹泻)的发生率和严重程度均增加。对于服用药物过量引起的不良反应应给予对症治疗,特别是严重腹泻应给予及时的治疗。
临床试验:
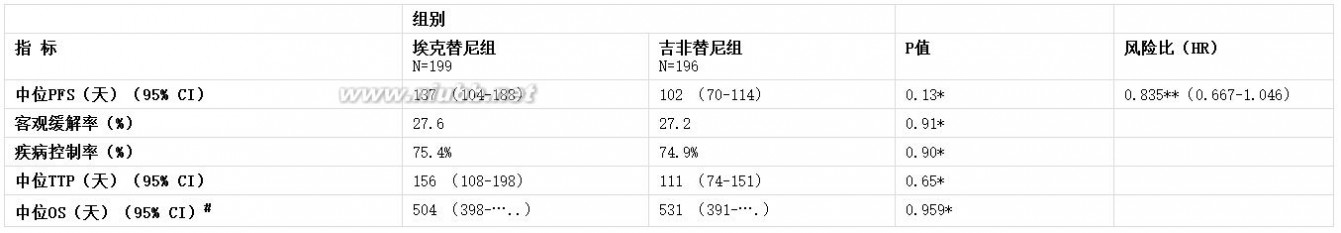
一项在中国27家临床研究机构中进行的随机、双盲双模拟、平行对照(1∶1)、多中心III期临床试验(ICOGEN),评价了埃克替尼和吉非替尼单药治疗既往接受过一个或两个化疗的局部晚期(IIIB或IV期)或转移的非小细胞肺癌(NSCLC)患者的疗效和安全性。受试者按1∶1随机分配接受埃克替尼125mg每天三次或吉非替尼250mg 每天一次口服给药,直至出现疾病进展或出现不能耐受的毒性。主要疗效指标为无进展生存期(PFS),次要疗效指标包括总生存期(OS)、客观缓解率(ORR)、疾病控制率(DCR)、疾病进展时间(TTP)以及生活质量(HRQoL)。
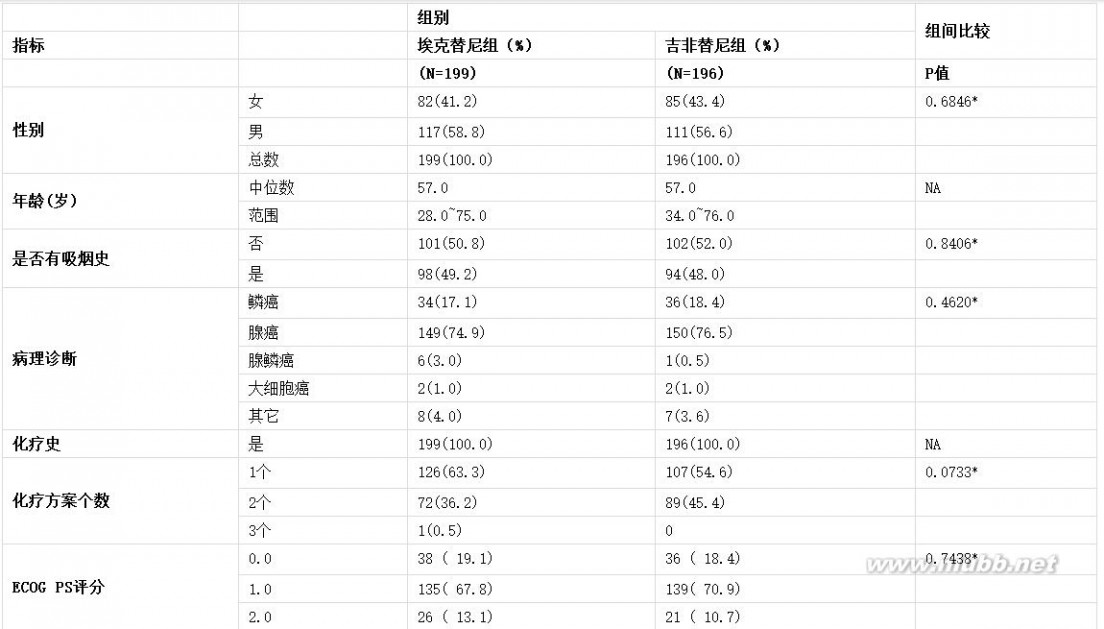
受试者的人口学资料和疾病特征比较分析情况见表3:
表3 ICOGEN试验两组间受试者的人口学资料和疾病特征比较

药代动力学:
本品分别在22例健康受试者和71例晚期NSCLC患者中分别进行了不同剂量单次和多次给药的药代动力学研究;口服后吸收迅速,分布广泛。平均血浆半衰期为约6小时,健康志愿者和癌症患者没有明显区别。埃克替尼口服7-11天后达到稳态,没有明显的蓄积。
吸收
药代动力学结果显示,晚期NSCLC患者单次口服125 mg剂量后埃克替尼吸收迅速,达峰时间在0.5-4 hr,平均Cmax分别为1400±547.52ng/mL,平均AUC0-last为3.4±1.21 hr?mg/L。
晚期NSCLC患者每日3次每次口服125 mg,连续7-11日即可达到稳态。达稳态以后,受试者单次服用125 mg后的达峰时间分别在1.5hr(0-4hr);平均Cmax为1860±721.84 ng/mL;平均AUC0-last为5.89±2.21 hr?mg/L。
在健康受试者中高热卡食物可显著增加其吸收,Cmax增加59%,AUC增加79%。在晚期NSCLC患者中没有比较食物对吸收的影响。
分布
晚期NSCLC患者单次口服150 mg(空腹服药)后,平均CL/F为13.3±4.78 L/hr;平均Vz/F为 115±63.26 L。125 mg剂量组肾累积排泄量Ae24h为0.234±0.1 mg。125 mg剂量组埃克替尼经尿排泄百分比分别为0.187%。
达到稳态后,晚期NSCLC患者单次服用125 mg后,肾累积排泄Ae8h为0.544±0.31 mg,埃克替尼经尿排泄百分比为0.436%。
空腹和餐后服用埃克替尼的平均分布容积分别为355L和113L,提示其在组织内分布广泛。
代谢
体外试验表明,埃克替尼主要通过细胞色素P-450单加氧酶系统的CYP2C19和CYP3A4代谢,对CYP2C9和CYP3A4有明显的抑制作用,未发现对大鼠肝P450酶明显诱导作用。(见【药物相互作用】)。
埃克替尼在人体主要经肝脏代谢,存在29种代谢产物,其中19种I相代谢产物,10种II相代谢产物。I相代谢反应为4-羟基喹啉环的侧链开环与开环后氧化反应、苯乙炔环15位羟基化和14位乙炔氧化,II相代谢反应为葡萄糖醛酸与硫酸结合反应。
单次给药时五种主要代谢产物Cmax总和为原药的19%~29%,其半衰期在5~16.5小时之间。多次连续给药后,五种主要代谢产物在7天左右达到稳态,其Cmax和AUC总和为原药的18%,谷浓度总和相当于原药的29%。
消除
空腹和餐后服用埃克替尼总的血浆清除率分别为46L/hr和22L/hr。主要通过粪便与尿液排泄(79.5%),其中粪便排泄占74.7%。排出形式以代谢产物为主(81.4%,),原型药物占18.6%。
尚未针对特殊人群如老年人、儿童、肝肾功能损伤人群进行药代动力学研究。
贮藏:
遮光、密封保存。
药品有效期:
12个月。
执行标准:
YBH02142011
说明书修订日期:
2011-06-07
二 : 凯尔丁说明书
通用名称:
盐酸洛非西定片
功能主治:
本品用于减轻或解除阿片类药物的戒断综合症。(www.61k.com]
用法用量:
开始用量为口服每次0.2mg,每日2次,以后可逐渐增加,每日增加0.2mg到0.4mg,最大可增至每日2.4mg,7~10天之后,再缓慢停药,至少要2至4天。
剂型:
片剂
不良反应:
洛非西定口服后主要的不良反应有瞌睡和口、咽及鼻腔干燥,困倦、乏力,此外还可能出现体位性低血压或短暂昏厥,这些反应在减少服药量后可自行消失。
禁忌:
凡血压低于90/40mmHg或心率低于60次/分时不应使用。对本品过敏者也不能应用。
注意事项:
1.有下列疾病的患者应当慎用:低血压、脑血管疾病、缺血性心脏病(包括近期的心肌梗死)、心动过缓、肾功不全以及有抑郁病史者。
2.因本品有中枢抑制作用,可引起瞌睡,服药者不宜驾车或操纵机器,以免发生意外。
3.本品必须缓慢(至少要2~4天,甚至更长)停药,以免突停发生反跳性血压升高。
成份:
本品主要成分盐酸洛非西定。
孕妇及哺乳期妇女用药:
安全性尚未建立。
儿童用药:
尚不明确。
药物相互作用:
因为本品为α2受体激动剂,所以不能与α受体阻断同时使用,以免发生药理学的拮抗作用。
药理作用:
药理学本品为咪唑啉类衍生物。与可乐定的结构和作用相似。选择性激动中枢?2受体,降低外周交感神经活性,抑制去甲肾上腺素释放,松弛血管平滑肌,产生血压下降作用。阿片类药物能抑制中枢去甲肾上腺素能神经原的活性,当戒除阿片药品或毒品时,因突然除去对该神经原的抑制而使其活动亢进,产生阿片类戒断综合症。本品能对抗这种作用,所以使用本品可使海洛因戒断综合征的强度与持续时间。本品无成瘾性。毒理学在大鼠和犬12月的口服毒性研究证明,洛非西定的用量在1mg/kg以下时没发现任何不良反应;3mg/kg是临界毒性剂量,这个剂量相当人治疗剂量的300倍;5.0~25.0mg/kg,相当于人治疗剂量的500~2500倍,出现中度到重度反应。可见这个药物的毒性不大,是比较安全的。
三 : 特罗凯说明书
特罗凯说明书
【批准文号】
注册证号H20060108
【中文名称】
盐酸厄洛替尼片
【产品英文名称】
ErlotinibHydrochlorideTablets
【生产企业】【功效主治】
Tarceva用于两个或两个以上化疗方案失败的局部晚期或转移的非小细胞肺癌的三线治疗。[www.61k.com)
【化学成分】
每片内含150mg厄洛替尼(以盐酸厄洛替尼形式存在)。
【药理作用】
Tarceva的抗肿瘤作用机制主要为抑制表皮生长因子(EGFR)酪氨酸激酶胞内磷酸化。
【药物相互作用】http://www.ntvcbbs.com
【不良反应】
最常见的不良反应是皮疹和腹泻,3/4度皮疹和腹泻的发生率分别为9%和6%,皮疹的中位出现时间是8天,腹泻中位出现时间为12天。发生率大于10%的不良反应有:皮疹、腹泻、食欲减低、疲劳、呼吸困难、咳嗽、恶心、感染、呕吐、口腔炎、瘙痒、皮肤干燥、结膜炎、角膜结膜炎、腹痛。肺毒性:有较少的报道提示在接受Tarceva治疗的NSCLC患者或其他实体瘤患者中可出现严重的间质性肺病(ILD),甚至导致死亡。在随机对照研究中,ILD的发生率是0.8%,并且这一发生率在Tarceva治疗组和安慰剂组是相同的。报道的ILD包括:肺炎、间质性肺炎、间质性肺病、闭塞性细支气管炎、肺纤维化、急性呼吸应激综合征和肺渗出。症状发生于治疗后5天~超过9个月,中位发生时间为47天。多数患者常有混杂因素导致ILD发生,如:之前有化疗/放疗、原有实质性肺疾病、肺转移或肺部感染。当有新出现的、难以解释的肺部症状,例如:呼吸困难、咳嗽、发热等,需进行检查评价,一旦诊断ILD,应停止继续使用Tarceva,并采取适当治疗。肝毒性:Tarceva治疗可引起无症状的肝转氨酶升高,因此,治疗期间应定期复查肝功能,包括:转氨酶、胆红素、碱性磷酸酶等,如果肝功能损害严重应减量或停药。肝功能损害常为暂时性的或伴有肝转移。较少报道有胃肠道出血,常发生于同时应用华法林的患者,所以,同时服用华法林或其他抗凝剂的患者应监测凝血酶原时间。老年患者:安
特罗凯价格 特罗凯说明书
全性和药代动力学在年轻人和老年患者中无明显差异,因此,应用于老年患者时不建议调整剂量。[www.61k.com]
【禁忌症】
对本品及成份过敏者禁用。
【产品规格】
150mg
【用法用量】
本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。厄洛替尼单药用于非小细胞肺癌的推荐剂量为150mg/日,至少在进食前1小时或进食后2小时服用。持续用药直到疾病进展或出现不能耐受的毒性反应。无证据表明进展后继续治疗能使患者受益。
【贮藏方法】
25℃保存,15℃~30℃之间也可接受。
【注意事项】
本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
特罗凯价格 特罗凯说明书
特罗凯

http://www.027116.com
【药品名称】
商品名:通用名:盐酸厄洛替尼片
【规格】150mg
【生产厂家】罗氏集团
【适应症】用于两个或两个以上化疗方案失败的局部晚期或转移的的三线治疗。[www.61k.com]
【用法与用量】本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
厄洛替尼单药用于非小细胞肺癌的推荐剂量为150mg/日,至少在进食前1小时或进食后2小时服用。持续用药直到疾病进展或出现不能耐受的毒性反应。无证据表明进展后继续治疗能使患者受益。
【规格】150mg
【生产厂家】罗氏集团
【适应症】用于两个或两个以上化疗方案失败的局部晚期或转移的的三线治疗。
【用法与用量】本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
厄洛替尼单药用于非小细胞肺癌的推荐剂量为150mg/日,至少在进食前1小时或进食后2小时服用。持续用药直到疾病进展或出现不能耐受的毒性反应。无证据表明进展后继续治疗能使患者受益。
【成份】每片内含150mg厄洛替尼(以盐酸厄洛替尼形式存在)
【性状】圆形、双凸、白色包衣片,一面印有棕色"T"和"150",另一面空白。
【药代动力学】
Tarceva口服后60%吸收,半衰期约36小时,主要由CYP3A4代谢清除。口服Tarceva150mg的生物利用度约60%,4小时后达血浆峰浓度。对591例接受单药Tarceva治疗的药代动力学分析显示,达到稳定血药浓度需7-8天,患者的年龄、体重、性别与药物的清除速率无显著关系,吸烟可使药物清除率增加24%。
特罗凯价格 特罗凯说明书
【禁忌症】对本品及成份过敏者禁用。[www.61k.com)
【不良反应】
最常见的不良反应是皮疹和腹泻,3/4度皮疹和腹泻的发生率分别为9%和6%,皮疹的中位出现时间是8天,腹泻中位出现时间为12天。
发生率大于10%的不良反应有:皮疹、腹泻、食欲减低、疲劳、呼吸困难、咳嗽、恶心、感染、呕吐、口腔炎、瘙痒、皮肤干燥、结膜炎、角膜结膜炎、腹痛。
肺毒性:
有较少的报道提示在接受Tarceva治疗的NSCLC患者或其他实体瘤患者中可出现严重的间质性肺病(ILD),甚至导致死亡。在随机对照研究中,ILD的发生率是0.8%,并且这一发生率在Tarceva治疗组和安慰剂组是相同的。报道的ILD包括:肺炎、间质性肺炎、间质性肺病、闭塞性细支气管炎、肺纤维化、急性呼吸应激综合征和肺渗出。症状发生于治疗后5天~超过9个月,中位发生时间为47天。多数患者常有混杂因素导致ILD发生,如:之前有化疗/放疗、原有实质性肺疾病、肺转移或肺部感染。当有新出现的、难以解释的肺部症状,例如:呼吸困难、咳嗽、发热等,需进行检查评价,一旦诊断ILD,应停止继续使用Tarceva,并采取适当治疗。
肝毒性:
Tarceva治疗可引起无症状的肝转氨酶升高,因此,治疗期间应定期复查肝功能,包括:转氨酶、胆红素、碱性磷酸酶等,如果肝功能损害严重应减量或停药。肝功能损害常为暂时性的或伴有肝转移。
61阅读提醒您本文地址:
较少报道有胃肠道出血,常发生于同时应用华法林的患者,所以,同时服用华法林或其他抗凝剂的患者应监测凝血酶原时间。
老年患者:
安全性和药代动力学在年轻人和老年患者中无明显差异,因此,应用于老年患者时不建议调整剂量。
【注意事项】本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
【贮存】25℃保存,15℃~30℃之间也可接受。
【包装】PVC泡罩包装;30片/盒。
【有效期】36个月
【进口药品注册证号】H20060108
【生产企业】RochePharma(Schweiz)Ltd.
本文由特罗凯格列卫整理!
61阅读提醒您本文地址:
四 : 印度特罗凯中文说明书
印度特罗凯中文说明书
【药品名称】
商品名:特罗凯
[1]通用名:盐酸厄洛替尼片
英文商品名:Tavceva
英文通用名:Erlotinib HCL Tablets
份子结构名:盐酸厄洛替尼片
化学名称:N-(3-乙炔苯基)-6,7-双(2-甲氧乙氧基)-4-喹啉胺盐酸盐
化学结构式:分子式:C22H23N3O4·HCl分子量:429.90
【成份】每片内含150mg厄洛替尼(以盐酸厄洛替尼形式存在)
【性状】圆形、双凸、白色包衣片。[www.61k.com)
【作用机制】
Tarceva的抗肿瘤作用机制主要为抑制表皮生长因子(EGFR)酪氨酸激酶胞内磷酸化。
【药代动力学】
Tarceva口服后60%吸收,半衰期约36小时,主要由CYP3A4代谢清除。口服Tarceva150mg的生物利用度约60%,4小时后达血浆峰浓度。对591例接受单药Tarceva治疗的药代动力学分析显示,达到稳定血药浓度需7-8 天,患者的年龄、体重、性别与药物的清除速率无显著关系,吸烟可使药物清除率增加24%。
【适应症】
Tarceva用于两个或两个以上化疗方案失败的局部晚期或转移的非小细胞肺癌的三线治疗。
【禁忌症】对本品及成份过敏者禁用。
【不良反应】
最常见的不良反应是皮疹和腹泻,3/4度皮疹和腹泻的发生率分别为9%和6%,皮疹的中位出现时间是8天,腹泻中位出现时间为12天。
发生率大于10%的不良反应有:皮疹、腹泻、食欲减低、疲劳、呼吸困难、咳嗽、恶心、感染、呕吐、口腔炎、瘙痒、皮肤干燥、结膜炎、角膜结膜炎、腹痛。 肺毒性:
有较少的报道提示在接受Tarceva治疗的NSCLC患者或其他实体瘤患者中可出现严重的间质性肺病(ILD),甚至导致死亡。在随机对照研究中,ILD的发生率是0.8%,并且这一发生率在Tarceva治疗组和安慰剂组是相同的。报道的ILD包括:肺炎、间质性肺炎、间质性肺病、闭塞性细支气管炎、肺纤维化、急性呼吸应激综合征和肺渗出。症状发生于治疗后5天~超过9个月,中位发生时间为47天。多数患者常有混杂因素导致ILD发生,如:之前有化疗/放疗、原有实质性肺疾病、肺转移或肺部感染。当有新出现的、难以解释的肺部症状,例如:呼吸困难、咳嗽、发热等,需进行检查评价,一旦诊断ILD,应停止继续使用Tarceva,并采取适当治疗。
肝毒性:
Tarceva治疗可引起无症状的肝转氨酶升高,因此,治疗期间应定期复查肝功能,包括:转氨酶、胆红素、碱性磷酸酶等,如果肝功能损害严重应减量或停药。肝功能损害常为暂时性的或伴有肝转移。
较少报道有胃肠道出血,常发生于同时应用华法林的患者,所以,同时服用华法林或其他抗凝剂的患者应监测凝血酶原时间。
1
特罗凯说明书 印度特罗凯中文说明书
老年患者:
安全性和药代动力学在年轻人和老年患者中无明显差异,因此,应用于老年患者时不建议调整剂量。[www.61k.com)
【肺 毒 性】
有较少的报道提示在接受Tarceva治疗的NSCLC患者或其他实体瘤患者中可出现严重的间质性肺病(ILD),甚至导致死亡。在随机对照研究中,ILD的发生率是0.8%,并且这一发生率在Tarceva治疗组和安慰剂组是相同的。报道的ILD包括:肺炎、间质性肺炎、间质性肺病、闭塞性细支气管炎、肺纤维化、急性呼吸应激综合征和肺渗出。症状发生于治疗后5天~超过9个月,中位发生时间为47天。多数患者常有混杂因素导致ILD发生,如:之前有化疗/放疗、原有实质性肺疾病、肺转移或肺部感染。当有新出现的、难以解释的肺部症状,例如:呼吸困难、咳嗽、发热等,需进行检查评价,一旦诊断ILD,应停止继续使用Tarceva,并采取适当治疗。
【肝 毒 性】
特罗凯Tarceva治疗可引起无症状的肝转氨酶升高,因此,治疗期间应定期复查肝功能,包括:转氨酶、胆红素、碱性磷酸酶等,如果肝功能损害严重应减量或停药。肝功能损害常为暂时性的或伴有肝转移。
较少报道有胃肠道出血,常发生于同时应用华法林的患者,所以,同时服用华法林或其他抗凝剂的患者应监测凝血酶原时间。
【老年患者】
安全性和药代动力学在年轻人和老年患者中无明显差异,因此,应用于老年患者时不建议调整剂量。
【注意事项】本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
【用法与用量】本品必须在有此类药物使用经验的医生指导下使用,并仅在国家肿瘤药物临床试验基地或三级甲等医院使用。
厄洛替尼单药用于非小细胞肺癌的推荐剂量为150mg/日,至少在进食前1小时或进食后2小时服用。持续用药直到疾病进展或出现不能耐受的毒性反应。无证据表明进展后继续治疗能使患者受益。
【规 格】150mg
【贮 存】
25℃保存,15℃~30℃之间也可接受。
【包 装】PVC泡罩包装;30片/盒。
【新包】7片/盒
【有效期】36个月
【进口药品注册证号】H20060108
【生产企业】Roche Pharma(Schweiz)Ltd.
特罗凯的作用机理是什么?
特罗凯的作用途径与化疗不同,是一种靶向治疗药物,可特异性地针对肿瘤细胞作用,抑制肿瘤的形成和生长。它是一种小分子化合物,可抑制人表皮生长因子受体(EGFR)的信号传导途径;是表皮生长因子(又可称HER1)信号传导通路的关键组分,在多种肿瘤细胞的形成及生长中都扮演了重要的角色。特罗凯的通过抑制酪氨酸激酶的活性的方式来抑制肿瘤生长,酪氨酸激酶是EGFR细胞内的重要组成部分之一。
2
五 : 特罗凯服用说明(转自与癌共舞网)
由于最近母亲病情有进展,而且胃和心脏都也出现了状况,以前一直有吃辅酶Q10,我走之前吃完了,家里还有硫酸锌,还有其他的保健药,我就没有再买,发现这个药吃特罗凯的时候也是不能停的。如果用冲击疗法的时候必须对胃进行保护,最严重的话会胃穿孔。150毫克已经是最大耐受量,万不得已不要轻易使用冲击疗法。
特罗凯TARCEVA;(厄洛替尼[erlotinib])口服片
2011-12-28,老马编辑
1. 剂型和规格:25 mg,100 mg和150 mg每片
2. 剂量和给药方法:应空腹服用特罗凯所有剂量至少进食前1小时或后2小时。
3. 警告和注意事项(包括以下几点,但不限于):
(1)曾不常报道间质性肺疾病(ILD)-样事件,包括死亡。如发生急性发作新或不能解释进展性肺症状,例如呼吸困难,咳嗽和发热中断特罗凯,如诊断为ILD终止特罗凯。
(2)脱水事件时中断特罗凯。监视脱水风险患者肾功能和电解质。
(3)如肝功能变化严重中断或终止特罗凯。如总胆红素>3 ×ULN和/或转氨酶>5 × ULN正常治疗前值时应中断或终止特罗凯给药。
(4)曾报道胃肠道穿孔,包括死亡。终止特罗凯。
(5)曾报道大疱和剥脱性皮肤病,包括死亡。中断或终止特罗凯。
4. 不良反应及处理:
在二线NSCLC治疗时最常见不良反应(>20%)是皮疹,腹泻,厌食,疲劳,呼吸困难,咳嗽,恶心,感染和呕吐。
(1)皮疹:
穿宽松、柔软、低领、棉质的衣服,局部皮肤应避免抓挠,勿用碱性肥皂和刺激性洗涤物及粗糙毛巾擦洗,保持皮肤清洁,外出时避免强烈日光照射,皮肤干燥可涂用润肤剂,皮肤瘙痒可口服抗组胺药物,如息斯敏(阿司咪唑)。
轻度皮疹可以局部涂搽百多邦(莫匹罗星软膏)或比亚芬(三乙醇胺乳膏),嘴唇四周可用蜂蜜涂抹。中度皮疹可以口服多西环素(强力霉素)或美满(米诺环素),100mg每日二次,这两种四环素类药物副作用较大,请谨慎使用。
(2)腹泻
轻者可予思密达口服,严重者予易蒙停(洛哌丁胺)2mg口服,每隔2小时1次,至腹泻停止12小时后停用。如严重腹泻,用洛哌丁胺无效或出现脱水,则需要减少特罗凯的剂量或暂时停止治疗。监测水、电解质变化,适当补充水、电解质,维持机体平衡,协助生活护理,鼓励患者多休息,进清淡易消化食物,便后注意肛周护理。
(3)恶心、呕吐
进清淡易消化食物,少量多餐,少吃甜食和易产气的食物,按医嘱予胃复安类药物口服。
(4)口腔黏膜炎
保持口腔清洁,早、晚用软毛刷刷牙,餐后漱口;避免进刺激性食物,必要时予复达欣、甲硝唑抗炎治疗。口腔局部可用蜂蜜涂抹。
(5)转氨酶升高
水飞蓟素(利加隆)、水飞蓟宾(水林佳)
(6)甲沟炎
避免向指甲加压,避免剪指/趾甲太短,不要穿紧鞋。轻度可用金银花水泡脚/手,百多邦、达维邦(环丙沙星)或立思汀(夫西地酸)外涂,每日1~2次。严重者可剪除嵌甲,清除甲下积脓,并用生理盐水清洗,然后用2%碘酊浸润脚趾20分钟,或用硝酸银无菌湿敷。
(7)心脏毒性
靶向药物会引起心脏毒性,药物性心脏毒性主要表现为胸闷、心悸、呼吸困难、心电图异常、LVEF下降以及心肌酶谱的变化,甚至导致致命性的心衰。可以通过临床症状结合心电图、超声心动图等检查进行诊断。可服用心脏保护剂预防,比如辅酶Q10。
5. 药物相互作用:
(1)CYP3A4抑制剂可能增加特罗凯血浆浓度。
正在用特罗凯与一种强CYP3A4抑制剂患者中例如,但不限于,阿扎那韦[atazanavir],克拉霉素[clarithromycin],印地那韦[indinavir],伊曲康唑[itraconazole],酮康唑[ketoconazole],萘法唑酮[nefazodone],那非那韦[nelfinavir],利托那韦[ritonavir],沙奎那韦[saquinavir],泰利霉素[telithromycin],醋竹桃霉素[troleandomycin,TAO],伏立康唑[voriconazole],或葡萄柚或葡萄柚汁,如发生严重不良反应应考虑减低剂量。相似地, in患者who aretaking特罗凯与一种CYP3A4和CYP1A2二者的抑制剂像环丙沙星[ciprofloxacin],如发生严重不良反应应考虑减低特罗凯剂量。
(2)CYP3A4诱导剂可能减低厄洛替尼血浆浓度。
治疗前用CYP3A4诱导剂利福平[rifampicin]减低厄洛替尼AUC约2/3至4/5。强烈建议用另一种缺乏CYP3A4诱导活性治疗。如不能得到另外治疗,在2周间隔当监视患者的安全性耐受时应考虑增加特罗凯剂量。特罗凯与利福平研究最大剂量是450mg。如特罗凯剂量向上调整,t终止利福平或其它诱导剂时,需立即减低剂量至使用的开始剂量。其它CYP3A4诱导剂包括,但不限于利福布丁[rifabutin],利福喷丁[rifapentine],苯妥英[phenytoin],卡马西平[carbamazepine],糖皮质激素药物(强的松>考的松>地塞米松),苯巴比妥[phenobarbital]和圣约翰草。
(3)CYP1A2诱导剂可能减低特罗凯血浆浓度。
(4)特罗凯溶解度是pH依赖性。改变上GI道pH的药物可能改变特罗凯的溶解度因而其吸收。
(5)吸烟减低特罗凯血浆浓度。
曾显示吸烟减低厄洛替尼暴露。应建议患者停止吸烟。如患者吸烟,小心增加特罗凯剂量,可考虑不要超过300mg,监视患者安全性。
注:涉及药物代谢的CYP主要为CYP1、CYP2、CYP3 3个家族中7种重要的亚型:CYP1A2、CYP2A6、 CYP2C9、CYP2C19、CPY2D6、CYP2E1和CYP3A4。
抑制剂(inhibitors)药酶活性减弱,使其他药物或本身代谢减慢,占代谢性相互作用的70%。
诱导剂(inducers) 药酶活性增强,使其他药物或本身 代谢加速,占代谢性相互作用的23%
肝脏微粒体混合功能氧化酶系统,细胞色素P450氧化酶,简称P450酶。
(6)质子泵抑制剂
特罗凯的溶解度与pH值相关。pH值升高时,特罗凯的溶解性降低。特罗凯与质子泵抑制剂奥美拉唑合用,特罗凯暴露[AUC]和最大浓度[Cmax]分别降低了46%和61%。Tmax或半衰期无变化。因此,影响上消化道pH值的药物可能会改变特罗凯的溶解度,从而改变其生物利用度。在与这些药物同用时增加特罗凯的剂量不太可能补偿暴露量的减少。
6. 不宜同时服用的中药和食物
食物:芹菜、番木瓜、台湾阳桃、石榴、欧洲胡萝卜、橙、柠檬、葡萄柚、茴香、芥末、芥菜、大蒜。
中药:槲皮素、人参、银杏叶提取物。
保健品:维生素E、β胡萝卜素。
7. 提高免疫力的药物及保健品
胸腺肽α1(日达仙)、胸腺法新(和日、迈普斯、基泰)、胸腺五肽、香菇多糖、黄芪多糖、参附注射液、参芪注射液、灵芝多糖、螺旋藻、虫草、海参、破壁灵芝孢子粉、黄精、黄芪、山药、灵芝等。
8. 饮食
多吃富含维生素和微量元素的蔬果,避免吃油腻的食品(如肥肉、油炸食品),忌烟酒、咖啡、辣椒。应多选择优质蛋白来源的食物如鸡蛋、牛奶、深海鱼,限制植物蛋白的摄入(黄豆、豆浆),同时避免含有香精、色素及防腐剂等影响肾功能的食物或药物。
9.特罗凯与其它靶向药联用方案(非成熟方案,仅供参考)
(1)特罗凯+XL184
(2)特罗凯+阿瓦斯丁
(3)特罗凯+替莫措胺
10.特罗凯与力比泰等化疗药物联合使用
力比泰等化疗药物联用特罗凯以及先特罗凯后力比泰,效果并不理想。因为特罗凯导致对特敏感的肿瘤细胞停滞于G0/G1期,使其免受力比泰的毒性(S期),影响疗效。特罗凯不应于力比泰等化疗药物的化疗疗程前5天内及后2天内使用。
61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1