一 : 阪崎肠杆菌:阪崎肠杆菌-概述,阪崎肠杆菌-发现过程
阪崎肠杆菌(Enterobacter Sakazakii)是肠杆菌科的一种,1980年由黄色阴沟肠杆菌更名为阪崎肠杆菌。阪崎肠杆菌能引起严重的新生儿脑膜炎、小肠结肠炎和茵血症,死亡率高达50%以上。截止2011年,微生物学家尚不清楚阪崎肠杆菌的污染来源,但许多病例报告表明婴儿配方粉是发现的主要感染渠道。广东省工商局公布2012年一季度全省流通环节乳制品、含乳食品抽样检验结果,有两批次婴儿配方奶粉检出含有致病菌“阪崎肠杆菌”。
阪崎肠杆菌_阪崎肠杆菌 -概述
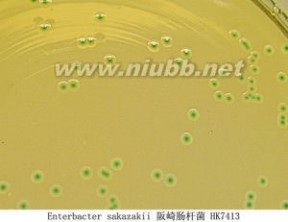 阪崎肠杆菌
阪崎肠杆菌阪崎肠杆菌(E.sakazakii)是人和动物肠道内寄生的1种革兰阴性无芽孢杆菌,属肠杆菌科肠杆菌属,是肠道正常菌丛中的1种,在一定条件下可引起人和动物致病。在1980年之前一直被称为黄色阴沟肠杆菌。随着对该菌认识的加深,根据阪崎肠杆菌与阴沟肠杆菌DNA、RNA杂交、生化反应、色素产生和抗生素敏感性的不同,研究人员对该菌的分类提出了质疑。
阪崎肠杆菌_阪崎肠杆菌 -发现过程
1961年,Franklin等首次报道了2例由阪崎肠杆菌引起的脑膜炎病例。以后相继在世界范围内(美国、冰岛、荷兰等国家)报道了一系列新生儿阪崎肠杆菌感染事件。
1976年Steigerwah等发现肠杆菌属菌株可分为与“黄色素存在或缺失”相关的2种不同的DNA杂交群。
1977年Brenner等发现可根据D一山梨醇产酸和延迟产生脱氧核糖核酸酶区分产色素和不产色素的菌株。
1980年Farmer等建议对产黄色素的阴沟肠杆菌重新分类,在同一篇文献中Farmer等指出通过DNA—DNA杂交他们发现阪崎肠杆菌之间DNA一致性可达83%一89%,而阪崎肠杆菌与阴沟肠杆菌的DNA共有序列只有31%一49%。
阪崎肠杆菌能引起严重的新生儿脑膜炎、小肠结肠炎和菌血症,并且可引起神经系统后遗症和死亡,该菌感染引起的死亡率高达50%以上。截止2011年,虽然还不能确定阪崎肠杆菌的宿主和传播模型,但在一些新生儿阪崎肠杆菌感染事件的调查中发现婴儿配方粉是主要的感染渠道。
阪崎肠杆菌_阪崎肠杆菌 -生物学性状
培养特征
 阪崎肠杆菌
阪崎肠杆菌阪崎肠杆菌兼性厌氧,营养要求不高,能在营养琼脂、血平板、麦康凯(MacConkey,MAC)琼脂、伊红美蓝琼脂、脱氧胆酸琼脂等多种培养基上生长繁殖。
所有的阪崎肠杆菌都能在胰蛋白酶大豆琼脂上36℃快速生长,24小时后形成直径2~3mm的菌落;25℃生长24h后形成直径1~1.5mm的菌落,48小时后形成直径2~3mm的菌落。Farmer等发现阪崎肠杆菌在结晶紫中性红胆盐葡萄糖琼脂平板上首次划线分离时,生长24小时后可生成两种或两种以上的菌落形态,1种干燥或粘液样,周边呈放射状,用接种环触碰可发现菌落极富弹性;另1种是典型的光滑型菌落,极易被接种环移动。截止2009年,尚不清楚这2种不同的菌落是否存在毒力和其它表型上的差别。Farmer等发现在TSA平板上培养24小时后,所有的阪崎肠杆菌都产生大量的沉淀物,像是包含团状细胞和无定形组织。
生化反应
Muytjens等研究了阪崎肠杆菌和相关菌株的酶反应特点。在对229株(其中129株是阪崎肠杆菌)细菌的研究中发现阪崎肠杆菌和其它肠杆菌之间存在2个主要的不同:阪崎肠杆菌a-葡萄糖苷酶活性均为阳性,其它肠杆菌均为阴性(包括产气肠杆菌)、阴沟肠杆菌、成团肠杆菌;所有试验菌株中只有阪崎肠杆菌缺少磷酰胺酶。
1985年Farmer等又检测了57株阪崎肠杆菌,其中53株a-葡萄糖苷酶活性为阳性。由此认为,a-葡萄糖苷酶是用来快速区分阪崎肠杆菌和其它肠杆菌的可靠方法。1983年Aldova等评估了从捷克斯洛伐克分离的73株阪崎肠杆菌吐温80脂酶的活性,结果显示97.3%的菌株含有该酶。
1984年Postupa和Aldova研究了从奶粉和婴儿配方粉中分离到的6株阪崎肠杆菌,发现所有的菌株在25℃和37℃培养7d后都产生吐温80脂酶。大量的研究结果表明,阪崎肠杆菌的生化反应与阴沟肠杆菌相似。在鉴定阪崎肠杆菌时需注意,该菌总是氧化酶阴性、D一山梨醇阴性、产生吐温80脂酶、细胞外DNAse阳性并形成黄色菌落。
抵抗力
Nazarowec-White等的早期研究认为婴儿配方粉中阪崎肠杆菌的污染与该菌的高度耐热性有关。然而,Breeuwer等研究发现阪崎肠杆菌并非具有特殊的耐热性,但能耐受一定程度的渗透压和干燥。无论是Nazarowec.White等还是Breeu.wer等人的研究结果都证明,阪崎肠杆菌的耐热性不足以使该菌经标准的巴斯德消毒后幸存,产品的污染很可能发生在干燥和罐装阶段。与大肠埃希菌、沙门菌相比,阪崎肠杆菌对渗透压和干燥具有更高的耐受力,这很可能与细胞内大量的海藻糖酶有关。
Edelson.Mammel和Buchanan研究了人工污染阪崎肠杆菌(根据生产商推荐的冲调方法,配方粉稀释液阪崎肠杆菌浓度约为106CFU/m1)的婴儿配方粉长期存放时细菌的生存态。在将近一年半中配方粉室温放置在1个密闭的带盖瓶子中,定期从中取样做定量检测,在最初的五个月内,阪崎肠杆菌活菌数量下降了2.5logCFU/ml(从6.0logCFU/ml下降到3.5logCFU/m1),每月约下降0.5logCFu/ml。随后的1年内阪崎肠杆菌活菌数量又下降了0.5logCFU/ml,终浓度约3.0logCFU/ml。该结果证明阪崎肠杆菌能在婴儿配方粉中长期存活。
增殖能力
阪崎肠杆菌的传代时间在6℃,21℃,37℃分别是13.7h,1.7h,19~21min。对阪崎肠杆菌进行危险性评估发现,与本底相比,25℃放置6小时该菌的相对危险性可增加30倍;25℃放置10小时可增加30000倍。
因此,即使婴儿配方粉中只有极微量的阪崎肠杆菌污染,在配方粉食用前的冲调期和储藏期该菌也可能会大量繁殖。2004年2月FAO/WHO在日内瓦召开的婴儿配方粉中阪崎肠杆菌专家研讨会上提出婴儿配方粉中微量的阪崎肠杆菌(<3CFU/100g)污染也能导致感染的发生。所以,对奶粉和婴儿配方粉的加工制作过程、家庭、医院的灭菌过程以及婴儿配方粉的储存和食用等关键控制点进行严格管理,是减少该类产品潜在危险性的重点。
毒力
国际上对阪崎肠杆菌的毒力因子和致病性知之甚少。Pagotto等在2003年首次描述了某些阪崎肠杆菌可能产生1种毒力因子1类肠毒素样化合物。组织培养发现一些菌株可产生细胞毒效应。腹腔注射剂量达108CFU/只时,18株试验株均可在3d内导致哺乳期小鼠死亡。经口灌胃,只有2株能引起哺乳期小鼠致死性损伤。SK92(肠毒素阳性)和MNW6(肠毒素阴性)腹腔注射致死剂量最小而在最大口服剂量时仍不能引起小鼠的致死性损伤。由此看来,阪崎肠杆菌之间的毒性存在明显不同,而且,某些菌株可能是非致病性的,这在某种程度上可能与细菌在胃的酸性环境中存活能力有关。
阪崎肠杆菌_阪崎肠杆菌 -生态分布
奶粉中的发现
 阪崎肠杆菌
阪崎肠杆菌婴儿配方粉的污染在多起阪崎肠杆菌感染的调查研究中发现,阪崎肠杆菌脑膜炎和婴儿配方粉紧密相关。
1988年,Muytjens等检测了从3五个国家收集的14一种婴儿配方粉,其中从十三个国家的二十种抽检样品中分离到阪崎肠杆菌(14.2%)。定量检测结果显示阪崎肠杆菌阳性样品的污染水平很低,除五种样品外,其他均低于1CFU/100g(0.36~0.92CFU/100g)。1983年Muytjens等从冲调好的配方奶中分离到阪崎肠杆菌,然而没有从冲调用的水和配方粉中分离到该菌。1984年Postupa和Aldova从捷克斯洛伐克的配方粉中分离到2株阪崎肠杆菌。
1990年Clark等调查了2起不相关的院内暴发的新生儿阪崎肠杆菌感染事件。在每起暴发中,都同时从病人和婴儿配方粉中分离到阪崎肠杆菌。采用多种分型方法(质粒分析、耐药谱、染色体限制性核酸内切酶分析、核糖体分型和多位点酶切电泳)对各株阪崎肠杆菌的相关性进行分析后发现虽然各分型方法不同,但在同一暴发事件中,从病人和配方粉中分离到的阪崎肠杆菌具有相同的特征。
2001年4月美国田纳西州发生阪崎肠杆菌感染事件后,医务人员与田纳西州健康和疾病控制中心协同对感染源进行了调查。对同一新生儿重症监护室中49例其他婴儿进行筛检,结果从10例婴儿体内分离到阪崎肠杆菌。为了查清感染源,研究人员对冲调配方粉的无菌水、已开罐的婴儿配方粉、同一批次未开罐的婴儿配方粉、用于冲调配方粉的用品等进行微生物学检测。无菌水和冲调用品阪崎肠杆菌检测为阴性,从未开罐和开罐的婴儿配方粉中分离到的阪崎肠杆菌脉冲场凝胶电泳指纹图谱与从脑膜炎患儿中分离到的相同。事件发生后,生产厂家在卫生部门的监督下收回了同一批次的所有产品,并对生产该批奶粉的工厂进行停产整顿。这是第一次因阪崎肠杆菌污染引起商业婴儿配方粉被广泛召回的报道。
2002年Block等报道了1999年12月至2000年月耶路撒冷一家医院发生的一起早产儿硝酸盐阴性阪崎肠杆菌感染事件。在这次感染中分离到的阪崎肠杆菌PFGE图谱完全一致,但与1993年~1998年的分离株不同。该菌没有从婴儿配方粉中分离出来,但是从已冲调的配方奶和厨房的搅拌器中分离到。停止使用该搅拌器后,对其重复进行阪崎肠杆菌检测发现至少五个月内仍可分离到阳性菌株,Block等因此认为搅拌器的阪崎肠杆菌污染可能来自该次感染事件发生之前使用的某批次的污染产品。更换使用另一厂家生产的婴儿配方粉,并隔离已感染的患儿后,感染得到有效的控制。
2011年12月23日,美国密苏里州2名婴儿食用美国强生婴幼儿配方奶粉后生病,其中一名婴儿不幸死亡,知名连锁商场沃尔玛决定全面下架该款奶粉,美强生则称奶粉出厂时未验出细菌,无安全问题。婴儿生病原因为感染阪崎肠杆菌。
环境分布
婴儿配方粉在制造过程中要经过巴斯德消毒,阪崎肠杆菌经过这样的处理后不可能继续存活。因此,终产品中阪崎肠杆菌的污染很可能是来自厂房环境、巴斯德消毒后添加热敏感性微量元素的过程或配方粉的冲调期。
对环境中阪崎肠杆菌的分布情况知之甚少。1990年Muyqens和Kollee为了解环境中阪崎肠杆菌的发生率,对其进行了广泛调查,抽检样品包括地表水、土壤、泥浆、朽木、谷类、家畜、牛、生牛奶等,但未从抽检的样品中分离到阪崎肠杆菌。2002年Leclercq等从奶酪、碎牛肉、腊肠和蔬菜中分离到阪崎肠杆菌,但目前仍不能确定该菌的自然宿主。
2003年Hamilton等从厩螫蝇中肠中分离到阪崎肠杆菌,据此认为厩螫蝇幼虫肠道是阪崎肠杆菌的环境宿主之一。厩螫蝇在世界范围内广泛分布,以牛、马、狗、猪和人等的血液为食,在牛、猪或马的养殖场所可见该蝇,在牛棚更常见,这使牛奶的污染成为可能。流行病学研究发现厩螫蝇的地理分布和阪崎肠杆菌感染直接相关。国际上已有从实验室果蝇肠道内分离到阪崎肠杆菌的报道。美国一家疫情控制公司的技术报告中记载舍蝇中存在阪崎肠杆菌,但没有确切记录该菌究竟是在舍蝇体内还是体外。Hamilton等从以上报道推测昆虫很可能是阪崎肠杆菌的环境宿主。该结论意味着,为了从根本上减少阪崎肠杆菌的污染,除了要在生产和产品使用期间实施各项控制措施外,还要在医院和生产环境中加强对蝇的消杀工作。
2004年Kandhai等从九个工厂和十六个家庭(餐桌)取样147份进行阪崎肠杆菌的检测,检测结果显示不同的环境检出率各不相同,但差别无统计学意义。阪崎肠杆菌从奶粉、谷类、巧克力、马铃薯粉、意大利面食加工厂和家庭环境中的检出,为该菌在环境中的广泛分布提供了强有力的证据。在设计预防新生儿阪崎肠杆菌感染的措施时,应该考虑到阪崎肠杆菌环境分布的广泛性。
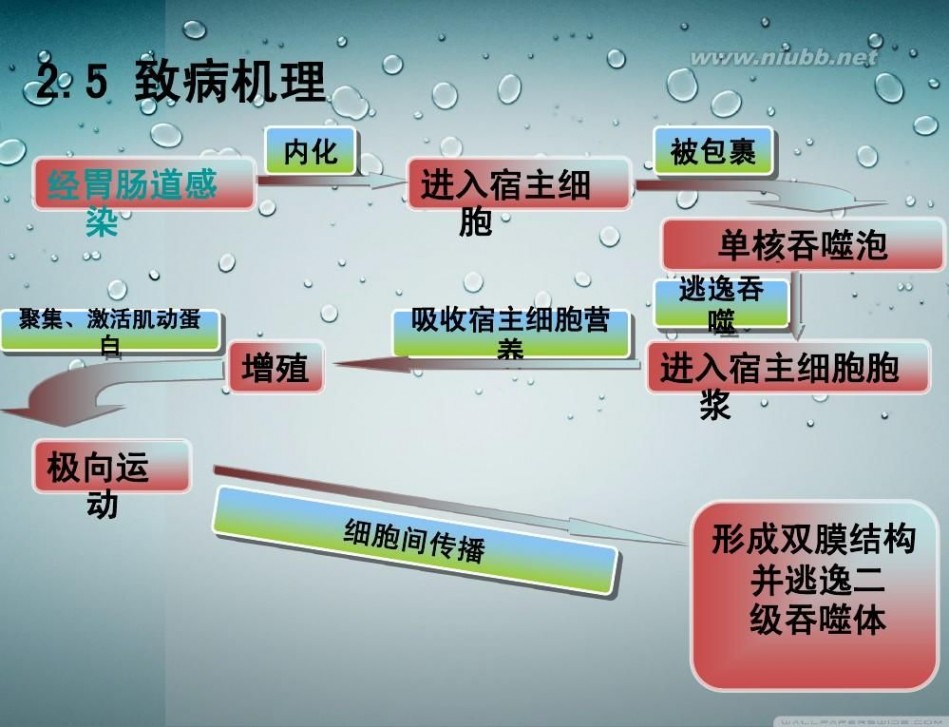
阪崎肠杆菌_阪崎肠杆菌 -致病物质
1、阪崎肠杆菌的毒力因子和致病性现在(截止2012年)还不太清楚,但已发现有些阪崎肠杆菌可能产生1种毒力因子-类肠毒素样化合物。而且,组织培养也发现一些菌株可产生细胞毒效应。
2、最近,TOWNSEND等发现婴儿配方奶粉中含有细菌脂多糖——内毒素(LPS),具有热稳定性,能增加小肠上皮细胞通透性,促使细菌侵入肠壁中而致病。
3、mange等通过体外组织细胞培养实验观察到阪崎肠杆菌对人类上皮细胞和脑微血管内皮细胞有吸附粘连特性,并形成丛生,表面形成生物保护膜。
4、由于阪崎肠杆菌细胞内含有大量的海藻糖酶,累积有大量的海藻糖,使得阪崎肠杆菌比沙门菌和其他肠杆菌更耐受渗透压和干燥。因阪崎肠杆菌这些特性,使得奶粉生产时不易杀灭,储存时易生存下来。
阪崎肠杆菌_阪崎肠杆菌 -致病性
阪崎肠杆菌感染的大多数病例都是婴儿,特别是早产儿、出生体重偏低等身体状况较差的新生儿。感染主要引起脑膜炎、脓血症、坏死性小肠结肠炎,阪崎肠杆菌引起的脑膜炎常引起脑梗塞、脑脓肿、囊肿形成和脑室炎等并发症,并且可引起神经系统后遗症或迅速死亡。除了感染新生儿外,该菌偶尔还可引起成人局部感染和菌血症等。
1、婴幼儿脑膜炎:未足月出生的新生儿占75%。主要表现为发热,面色苍白,有抽搐或颤抖,张力亢进,囱门隆出,无颈项强直。合并有菌血症者占5/8,坏死性小肠结肠炎占2/8,死亡率高达75%。阪崎肠杆菌引起的脑膜炎常引起脑梗塞、脑脓肿、囊肿形成和脑室炎等并发症,并且可引起神经系统后遗症或迅速死亡。
2、新生儿菌血症:寒战,白细胞偏低,血液培养分离可得到阪崎肠杆菌,多数症状较轻,如出现严重的脓毒血症,死亡率可达36%
3、新生儿坏死性小肠结肠炎(NEC):多发生于未足月出生体重较轻的婴幼儿。
4、成人感染:阪崎肠杆菌引起成人菌血症或局部感染。
阪崎肠杆菌_阪崎肠杆菌 -检查
1、不利用山梨醇。
2、36度下培养七天,DNA酶为阳性。
3、根据阪崎肠杆菌中寡-1,6-葡萄糖苷酶基因设计引物建立PCR方法,并进行PCR反应的灵敏度、特异性实验以及模拟实际样品的最低检出限测定。
阪崎肠杆菌_阪崎肠杆菌 -菌落特征
在胰蛋白胨琼脂(TSA)、脑心浸液琼脂(BHI)及血平板上经25~36℃培养24h后,形成1.5~2.5mm,黄色菌落,菌落形态有两种:1种为典型的光滑型菌落,极易被接种环移动,另1种为干燥或粘液样,周边呈放射状,不易被接种环移动,似橡胶状有弹性。后1种经传代后可转化为有光泽的菌落。
阪崎肠杆菌_阪崎肠杆菌 -培养温度
阪崎肠杆菌具有耐热及耐寒性,在外界环境中比其他肠道杆菌生存率强,培养最佳温度25—36℃,在6~45℃下都能生长,某些菌株可在47℃下生长。阪崎肠杆菌_阪崎肠杆菌 -菌落颜色
阪崎肠杆菌在MAC琼脂上为无色透明菌落,在TSA及BHI上生长为黄色菌落,在结晶紫中性红胆盐葡萄糖琼脂(VRBG)能产生紫红色菌落,而在TSA上加5-溴-4-氯-吲哚-α-D-吡喃葡萄苷(Xα-GLC)仅阪崎肠杆菌能产生兰绿色菌落,现已作为阪崎肠杆菌快速培养的选择性培养基,在4-甲基-伞形酮-α-D-葡萄糖苷(NA+α-MUG)培养基上产生荧光菌落。
阪崎肠杆菌_阪崎肠杆菌 -抵抗力
耐高温、干燥、渗透压
阪崎肠杆菌比其他肠杆菌耐高温,LEHNER研究发现阪崎肠杆菌在婴儿配方奶粉中60℃存活2.5min,并且72℃仍能存活。BREELLWER等观察阪崎肠杆菌在58℃下能持续0.39~0.60min不死。由于阪崎肠杆菌细胞内含有大量的海藻糖酶,累积有大量的海藻糖,使得阪崎肠杆菌比沙门菌和其他肠杆菌更耐受渗透压和干燥。因阪崎肠杆菌这些特性,使得奶粉生产时不易被杀灭,储存时易生存下来。
耐酸性
阪崎肠杆菌耐酸性并对清洁剂和杀菌剂有较强抵抗力。LEH—NER的实验表明,阪崎肠杆菌能在pH0.9~2下存活(胃部的酸性环境),可能与阪崎肠杆菌周身菌毛结构有关,该菌毛结构易使细菌形成共生集合体,也易粘附在各种物体表面形成一层生物保护膜,对清洁剂和杀菌剂具有较强的抵抗力。
阪崎肠杆菌_阪崎肠杆菌 -治疗
1、一般说来,与肠杆菌属其它细菌相比,阪崎肠杆菌对常用的抗菌药更敏感。
2、阪崎肠杆菌对先锋霉素1和新诺明之外的所有试验用药敏感,且该菌是唯一对氨比西林敏感的肠杆菌。
3、虽然阪崎肠杆菌的最佳抗生素治疗方法尚未确定,但在大数早期报告的病例中都是应用氨比西林和庆大霉素联合疗法。
阪崎肠杆菌_阪崎肠杆菌 -预防
1、婴儿出生的前6个月,母乳喂养最有助于婴儿的生长和健康。但是为了保证婴儿发育需要的营养,必须科学地补充喂养适宜的母乳代用品,如符合食品法典委员会(CAC)标准的婴儿配方食品。应对不能进行母乳喂养的婴幼儿,特别是高危人群提出警示:配方乳粉并不是灭菌产品,可能被病原体污染并引起疾病。
2、用商业无菌液体或开水冲调配方食品,喂食婴儿剩余的液体调配食品应放置冰箱保存,并在食用前再加热。
阪崎肠杆菌_阪崎肠杆菌 -控制方法
1、制定婴幼儿配方奶粉中阪崎肠杆菌微生物标准,建立有效控制措施,将其危险性降低到最低。
2、制定加工、使用和操作婴幼儿配方食品的导则,研究降低阪崎肠杆菌污染水平的方法,在生产环境和配方奶粉中降低阪崎肠杆菌的浓度和流行的危险性;为高危人群生产较大比例的商业无菌配方替代产品。
3、制定有效的环境监测计划,将肠杆菌科而不是大肠杆菌作为工业生产线的卫生指标菌。
4、建立实验室监测网络,对阪崎肠杆菌的来源、传播途径等进行调查研究;加强相关学科的基础研究,包括生态学、分类学、菌株毒力等。
5、用商业无菌液体或开水冲调配方食品,喂养婴幼儿后剩余的调配食品应放置冰箱保存,并在食用前再加热。我国应根据实际情况制定相应管理办法,加强对阪崎肠杆菌的检测技术及控制技术研究,进1步完善婴幼儿配方食品标准,以保证婴幼儿群体的健康与安全。
阪崎肠杆菌_阪崎肠杆菌 -生化反应
阪崎肠杆菌在定名前一直被伯杰分类为产黄色素的阴沟肠杆菌,实际上是阴沟肠杆菌的1个亚种,因此与阴沟肠杆菌的生化反应有许多相似的地方。阪崎肠杆菌与阴沟肠杆菌有31%~49%的DNA序列同源性,G+C含量为57%。
MUYTJENS等在对226株(其中129株为阪崎肠杆菌,其他为阴沟肠杆菌60株,产气肠杆菌19株,聚团肠杆菌18株)肠杆菌的研究中,发现阪崎肠杆菌和其他肠杆菌之间存在2个主要的不同:阪崎肠杆菌α-葡萄糖酶苷活性均阳性,而缺乏磷酰胺酶活性。由此认为,凭2种酶活性检测可将阪崎肠杆菌与其他肠杆菌明显地区分开来,并且将α-葡萄糖酶苷活性检测可用来快速分离阪崎肠杆菌。
POSTUPA研究了从婴儿配方奶粉中分离到的6株阪崎肠杆菌,发现所有的菌株都能产生吐温-80脂酶。因此,吐温-80脂酶活性测定也可以作为阪崎肠杆菌的鉴定依据。
阪崎肠杆菌_阪崎肠杆菌 -检测必备仪器--荧光pcr仪
实时荧光定量PCR检测系统也叫实时荧光定量核酸扩增检测系统(英文全名是Real-timeQuantitativePCRDetectionSystem),简称实时荧光QPCR,qPCR的核心是实时荧光定量PCR仪及与其配套的检测分析软件系统。
聚合酶链式反应(PolymeraseChainReaction简称PCR)原理凭借敏感、特异、快速的特点荣获1993年诺贝尔化学奖。因其在病原体检测方面的独特优势,因而发达国家在相关方法和仪器方面的研发非常快,成为分子生物学诊断的主流,至今仍处于学术和应用前沿,发展至今已有三代产品:第一代PCR定性检测技术及设备由基因扩增热循环仪(DNAThermalCycler)+电泳仪+紫外分析仪+定性试剂构成;第二代PCR-DNA终点定量技术及设备(End-pointquantitativePCRdetection)由基因扩增热循环仪+荧光仪+终点定量试剂构成,其又分为终点酶免定量(End-pointELISA-PCR)和终点荧光定量(End-pointFlour-PCR)2种;第三代产品为Real-timeqPCR-DNA/RNA实时荧光定量检测。
qPCR检测灵敏度高,检测线性范围宽,检测精度和重复性好等突出优势,因此被公认为目前世界用于临床及科研的最先进核酸分子诊断技术,被美国FDA承认并推崇。检测项目包括:食物等病原菌以及疾病病毒等病原体如:乙肝病毒HBVDNA,丙肝病毒HCVRNA,艾滋病病毒HIVRNA,沙眼衣原体CT,淋病双球菌NG,巨细胞病毒CMV,结核分支杆菌Mtb、禽流感、阪崎肠杆菌、口蹄疫、新城疫、猪瘟、大肠埃希菌O157∶H7、沙门菌、炭疽芽孢杆菌、胸膜肺炎放线杆菌、寄生虫病等。
PCR仪的应用范围广,几乎所有的生命科学领域都要涉及:食品检测、临床检验、疾病控制、检验检疫、科研实验室、食品安全、化妆品检测、环境卫生等。国内多家试剂厂商生产了包括肝炎、性病、优生优育、呼吸道疾病、禽流感、阪崎肠杆菌、口蹄疫、新城疫、猪瘟、大肠埃希菌O157∶H7、沙门菌、炭疽芽孢杆菌、胸膜肺炎放线杆菌、寄生虫病等在内的数10种荧光定量PCR试剂盒,购买方便,价格便宜,并获得了国家相关认证。
阪崎肠杆菌_阪崎肠杆菌 -近期动态
美国俄克拉荷马州一名婴儿被检测出对阪崎肠杆菌(Cronobacter)呈阳性反应,此前该病菌已导致一名婴儿死亡,另一名患病。美国目前正对婴儿配方奶粉进行调查。
美国疾病防控中心发言人BarbaraReynolds星期二表示,阪崎肠杆菌有时会导致新生儿罕见疾病,以前在婴儿配方奶粉中曾发现该细菌。
俄克拉荷马州卫生部的LesleaBennett-Webb称,最新检测出阳性反应的这名婴儿还不到1个月大,未食用过美赞臣(MeadJohnsonNutrition)(MJN.N:行情)Enfamil婴儿配方奶粉,入院治疗後已出院。
这是近几周发生的第三起阪崎肠杆菌病例,此前该病菌已导致密苏里州一名婴儿死亡,伊利诺伊州一名婴儿患病,目前正在康复中。 美国食品药物管理局称,密苏里州那名婴儿曾食用Enfamil配方奶粉,而伊利诺伊州那名婴儿曾食用Enfamil以及其它多种品牌配方奶粉。
沃尔玛(WMT.N:行情)等美国零售商已将Enfamil奶粉下架,但目前联邦调查人员尚未发现病例与该奶粉存在关联。
2005年5月20日,由中国检验检疫科学研究院和天津出入境检验检疫局牵头完成的《奶粉中阪崎肠杆菌检测方法》行业标准在京通过了审定。这项标准的出台,解决了我国检测婴幼儿配方奶粉中阪崎肠杆菌无标准、无检测方法的问题。10月该标准被实施。
该标准建立了阪崎肠杆菌的改进的传统检测方法、普通PCR方法和荧光PCR方法。
据了解,阪崎肠杆菌是乳制品中近几年新发现的1种致病菌。它是存在自然环境中的1种“条件致病菌”,已被世界卫生组织和许多国家确定为引起婴幼儿死亡的重要条件致病菌,可导致任何年龄层人群的疾病,尤其是对早产儿、出生体重轻的婴儿或免疫受损婴儿的威胁最大,严重者可导致败血症、脑膜炎或坏死性小肠结肠炎。
继美国FDA2002年在本土某一些国际乳业巨头生产的婴儿配方奶粉中检出阪崎肠杆菌后,2003年又一家国际乳业巨头公司主动召回在美国生产的一批检出极微量阪崎肠杆菌的罐装早产儿特殊配方奶粉,此后成为世界关注的焦点。我国在2005年5月通过《奶粉中阪崎肠杆菌检测方法》行业标准的审定,对奶粉严查此菌。
二 : 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌

李斯特菌感染 细菌食品中毒--李斯特菌,阪崎肠杆菌
61阅读提醒您本文地址:
三 : 阪崎肠杆菌研究进展_梁鹰

418
文章编号:10052376X(2008)0420418203
ChineseJournalofMicroecology,Aug2008,Vol120No14
【综 述】
阪崎肠杆菌研究进展
梁鹰,王红戟
(台州市路桥疾病预防控制中心,浙江台州 318050)
【摘要】 阪崎肠杆菌属肠杆菌科肠杆菌属,是人和动物肠道内寄生的一种革兰阴性无芽胞杆菌,属条件致病菌,能引起严重的新生儿脑膜炎、小肠结肠炎和菌血症,死亡率高达50%以上。(www.61k.com]阪崎肠杆菌耐酸、耐高温、耐干燥,对外界环境有较强的抵抗力。阪崎肠杆菌的微生物学检验方法,包括传统细菌学培养方法及各种基于聚合酶链反应(PCR)的分子生物学方法。
【关键词】 阪崎肠杆菌;条件致病菌;微生物学;检验方法
【中图分类号】R378.2 【文献标识码】A
ResearchprograssingofEnterobactersakazakii
LIANGYing,WANGHong2jie
(TaizhouCityLuqiaoDistrictCenterforDiseaseControlandPrevention,318050,【Abstract】 Enterobactersakazakii(E.sakazakii)isametheEnterilyEnterobac2teriaceae,whichisakindofgram2negativeandnon2sporebacillusal.Itisacondi2tionedpathogenandcancausesevereneonatalmeningitis,ia.ratesfromE.sakazakiiinfactionhavebeenreportedtobehigherthan50%.E.tohightemperature,acidanddryenvironment.Themainmicrobiolfincludesconventionalculturalmethodsand
variousmolecularbiologicalPCR.
【Keywords】 icroorganism;Detectionmethod
)是人和动物肠道内寄
,,一直被称为黄色阴沟杆菌PigmentedEnterobactercloacae)[1],直到1980年才由FARMER和他的同事[2]更名为阪崎肠杆菌。因阪崎肠杆菌是肠道正常菌群中的一种,属条件致病菌,一直未被临床引起重视,直到1961年,英国的URMENYI和
[3]
FRANKLIN两位医生首次报告了由该菌引起的两例脑膜炎病例,随后丹麦、美国、荷兰、希腊、冰岛、比利时等国家相继报道了新生儿阪崎肠杆菌感染事件。阪崎肠杆菌能引起严重的新生儿脑膜炎、菌血症和坏死性小肠结肠炎,并可能遗留严重的神经系统后遗症,死亡率20%~50%[2]。国外文献报道最多的是阪崎肠杆菌污染了婴儿配方奶粉,引起婴幼儿感染。也有几例成年人感染病例的报告[4]。阪崎肠杆菌分离检测方法,国际上通常以美国FDA2002年8月发布的“婴儿配方奶
[5]
粉中阪崎肠杆菌的分离计数”作为经典方法,在此基础上做了较多的改良方法及分子生物学检测方法。我国也与2005年8月颁布了奶粉中阪崎肠杆菌检测方法[6]。临床上对阪崎肠杆菌的病原学检测方法报告较少。本文就阪崎肠杆菌的主要微生物学特性,致病性,分离检测作一综合性介绍,以飧读者。1 阪崎肠杆菌微生物学特性1.1 形态染色 阪崎肠杆菌属肠杆菌科肠杆菌属,因此本菌具备肠杆菌基本形态特征:革兰阴性粗短杆菌,细胞大小为(0.6~1.1)×(1.2~3.0),有周身菌毛,无芽胞,有动力[7]。1.2 培养特性1.2.1 营养要求 不高,能在普通营养琼脂、血平板、麦康凯(MAC)琼脂、伊红美兰(EMB)琼脂、脱氧胆酸琼脂等多种培养基上生长繁殖。1.2.2 培养温度 阪崎肠杆菌具有耐热及耐寒性,在外界环境中比其他肠道杆菌生存率强,培养最佳温度25~36℃,在6~45℃下都能生长,某些菌株可在47℃下生长[8]。1.2.3 菌落特征 在胰蛋白胨琼脂(TSA)、脑心浸液琼脂(BHI)及血平板上经25~36℃培养24h后,形成1.5~2.5
[1]
mm,黄色菌落,菌落形态有2种:一种为典型的光滑型菌落,极易被接种环移动,另一种为干燥或粘液样,周边呈放射状,不易被接种环移动,似橡胶状有弹性。后一种经传代后可转化为有光泽的菌落[7]。1.2.4 菌落颜色 阪崎肠杆菌在MAC琼脂上为无色透明菌落,在TSA及BHI上生长为黄色菌落,在结晶紫中性红胆盐
【收稿日期】2008204203【作者简介】梁鹰(19572),男,工商管理碩士,副主任技师,从事微生物
检验葡萄糖琼脂(VRBG)能产生紫红色菌落,而在TSA上加52溴2
α2α2GLC)仅阪崎肠杆菌能产生兰42氯2吲哚2D2吡喃葡萄苷(X
绿色菌落,现已作为阪崎肠杆菌快速培养的选择性培养基[9],
α2在42甲基2伞形酮2D2葡萄糖苷(NA+α2MUG)培养基上产[10]
生荧光菌落。1.3 生化反应 阪崎肠杆菌在定名前一直被伯杰[1]分类为产黄色素的阴沟肠杆菌,实际上是阴沟肠杆菌的一个亚种,因此与阴沟肠杆菌的生化反应有许多相似的地方。阪崎肠杆菌与阴沟肠杆菌有31%~49%的DNA序列同源性,G+C含量为57%[2]。
[11]
MUYTJENS等在对226株(其中129株为阪崎肠杆菌,其他为阴沟肠杆菌60株,产气肠杆菌19株,聚团肠杆菌18株)肠杆菌的研究中,发现阪崎肠杆菌和其他肠杆菌之间存在两个主要的不同:阪崎肠杆菌α2葡萄糖酶苷活性均阳性,而缺乏磷酰胺酶活性。由此认为,凭两种酶活性检测可将贩崎肠杆菌与其他肠杆菌明显地区分开来,并且将α2葡萄糖酶苷活性检测可用来快速分离阪崎肠杆菌。
[12]
POSTUPA研究了从婴儿配方奶粉中分离到的6株阪崎肠杆菌,发现所有的菌株都能产生吐温280脂酶。因此,吐温280脂酶活性测定也可以作为阪崎肠杆菌的鉴定依据。1.4 抵抗力1.4.1 耐高温、干燥、渗透压 阪崎肠杆菌比其他肠杆菌耐
[13]
高温,LEHNER研究发现阪崎肠杆菌在婴儿配方奶粉中60℃存活2.5min,并且72℃仍能存活。BREELLWER等[8]观察阪崎肠杆菌在58℃下能持续0.39~0.60min不死。由于阪崎肠杆菌细胞内含有大量的海藻糖酶,累积有大量的海藻糖,使得阪崎肠杆菌比沙门菌和其他肠杆菌更耐受渗透压和干燥。因阪崎肠杆菌这些特性,使得奶粉生产时不易被杀灭,储存时易生存下来。
1.4.2 耐酸性并对清洁剂和杀菌剂有较强抵抗力 LEH2
[13]
NER的实验表明,阪崎肠杆菌能在pH0.9~2下存活(胃部的酸性环境),可能与阪崎肠杆菌周身菌毛结构有关,该菌毛结构易使细菌形成共生集合体,也易粘附在各种物体表面形成一层生物保护膜,对清洁剂和杀菌剂具有较强的抵抗力。2 阪崎肠杆菌临床意义
阪崎肠杆菌可引起各年龄段人群的疾病,但从已报道的病例年龄分布来看,婴幼儿(1岁以下的儿童)是该菌感染的高危人群,特别是新生儿、早产儿、出生体重偏低、免疫力低下等身体状况较差的婴儿。感染主要引起脑膜炎、脓毒血症、坏死性小肠结肠炎;阪崎肠杆菌引起的脑膜炎常引起脑梗塞、脑脓肿和脑室炎等併发症,并且可引起神经系统后遗症,死亡率较高。成人主要是引起局部感染和菌血症。2.1 致病因素 文献对阪崎肠杆菌的致病因素报道不多,所
阪崎肠杆菌 阪崎肠杆菌研究进展_梁鹰


中国微生态学杂志 2008年8月第20卷第4期
知甚少。[www.61k.com)目前所知阪崎肠杆菌致病性与类肠毒素和内毒素有关。PAGOTTO[14]首先描述阪崎肠杆菌可能产生一种毒力因子———类肠毒素样化合物,经腹腔注射板崎肠杆菌剂量达8
10CFU/只时。18株实验菌株均可导致乳鼠死亡,其中4例检测到类肠毒素样化合物。国内许龙岩等[15]观察小鼠在接种阪崎肠杆菌菌液6小时后出现中毒症状,8小时后中毒症状加深,24小时后全部死亡。经解剖发现实验鼠小肠肿胀,有气泡,肠壁变薄、糜烂,肠系膜血管、腹膜血管变粗、充血。
[16]
最近,TOWNSEND等发现婴儿配方奶粉中含有细菌脂多糖———内毒素(LPS),具有热稳定性,能增加小肠上皮细胞通透性,促使细菌侵入肠壁中而致病。他将纯化的肠杆菌属脂多糖与阪崎肠杆菌一起经注射入乳鼠腹腔中,能明显提高阪崎肠杆菌穿透血脑屏障的能力,该实验虽未明确表明阪崎肠杆菌产生内毒素,但推测阪崎肠杆菌的致病性与细菌内毒素有明显的关联。
[17]
MANGE等通过体外组织细胞培养实验观察到阪崎肠杆菌对人类上皮细胞和脑微血管内皮细胞有吸附粘连特性,并形成丛生,表面形成生物保护膜。
[18]
KIM等支持上述实验结果,他们利用不锈钢管、玻璃管及PVC塑料管腔内壁,只要有一定营养液和适宜温度崎肠杆菌就可以在这些管腔内吸附生存,,抵御消毒剂等的杀伤作用。2.2 所致疾病
[3]
2.2.1 FRANKLIN等首次报道了2(杆菌),起的婴幼儿脑膜炎1983年MUYTJENS等[19]对荷兰地区6年来发生的8例阪崎肠杆菌引发的婴幼儿脑膜炎作了回顾性调查分析。发现未足月出生的新生儿占75%,出生时低体重(<2000g)的新生儿易感染(6/8),并与人工喂养奶粉有关。主要症状:发热、面色苍白,有抽搐或颤抖,张力亢进,囱门隆出,无颈项强直。合併有菌血症者占5/8,坏死性小肠结肠炎占2/8,死亡率高达75%(6/8)。2例存活的病人中伴有严重的神经系统后遗症。在大部分病例的脑脊液和血液中分离到阪崎肠杆菌。Biering等[20]在1989年报告了3例住在冰岛首都国立大学附院新生儿重症监护室病人,1例正常出生但伴有左脑损伤,1例是Down′s综合症(先天性无肛门),另1例为健康的男性双胞胎之一,他们共同特征是人工喂养婴儿配方奶粉5天后发病,出现发热、精神萎靡、嗜睡、脑脊液可见大量的嗜中性粒细胞,培养分离均找到阪崎肠杆菌,除1例死亡外,1例发展为四肢瘫痪、痴呆,另1例为阵发性癫痫病。
[21]
BOWEN等分析46例阪崎肠杆菌感染的病例,其中脑膜炎的发病率是72%(33/42),在33例的脑膜炎病例中有33%发展为癫痫,21%有脑脓肿,死亡率42%。
2.2.2 新生儿菌血症 该病例最早报告的是在1979年,
[22]
MONROE发现一出生6天(体重2600g)的患儿出现低热(38.3℃)、寒颤,白细胞偏低,其血液培养分离到阪崎肠杆菌,经氨替比林治疗后痊愈,未发生脑膜炎。
阪崎肠杆菌感染新生儿发生的菌血症,据BOWEN[21]对46例该菌感染的新生儿分析,其发病率是38%(12/42)。多数症状较轻,如出现严重的脓毒血症,死亡率可达36%。2.2.3 新生儿坏死性小肠结肠炎(NEC) ACKER等[23]报告了比利时一家医院的新生儿重症监护室在1998年6~7月间共有12例阪崎肠杆菌引起的NEC暴发事件,12例NEC都经临床确诊,这些患儿的特点是:均未足月出生,体重全部低于2000g,最低体重590g,平均体重只有1177g,人工喂食奶粉。胃液分离到阪崎肠杆菌7例(7/12),肛指液分离到9例(9/12),血液分离到4例(4/12),死亡2例(2/12)。2.2.4 成人感染 阪崎肠杆菌引起成人感染的报告虽不很多,但从现有资料看涉及到成人各年龄段都有发生。本菌是条件致病菌,当机体因其他疾病导致免疫功能低下时,可引起菌血症、脓毒血症及泌尿道、呼吸道、创伤面感染,也可引起脑
[24]
膜炎、胆囊炎。周庭银等报告的3例阪崎肠杆菌感染其中败血症1例(女,45岁),尿路感染1例(女,55岁),中耳炎1例(男,21岁)。龚燕等[25]报告从64例痰液中分离到阪崎肠杆菌,其中有62例(96.7%患有基础疾病:慢性阻塞性肺疾病24例,呼衰7例,糖尿病6例,肺结核2例,肺癌2例,近期化
419
疗8例,肠梗阻2例)。最近,See等[26]报告一个75岁老妇患多发性脾脓肿合併阪崎肠杆菌菌血症。3 阪崎肠杆菌微生物学检验3.1 细菌学分离培养方法3.1.1 经典方法 所谓经典方法,即是美国FDA推荐[5]的“三管法”培养分离阪崎肠杆菌的方法。基本步骤如下:(1)以无菌称取100、10、1g婴儿配方奶粉用无菌蒸馏水以1∶10稀释,充分溶解后36℃24h孵育;(2)充分混匀后分别取10ml加入至装有90mlEE肉汤增菌培养36℃24h;(3)充分混匀后用直接涂布法或直接划线接种法,在VRBG平板中孵育36℃24h;(4)从每个VRBG平板中挑取5个可疑菌落,分别接种在TSA平板25℃48~72h;(5)在TSA平板上挑取黄色、无光泽典型菌落在API20E进行鉴定。该方法自2002年被推荐公布以来,方法,缺点是时间太长,需时7。
αGLC[11] 3.1.2 改良法该法是利
,在TSA培养基
2αGLC)作为发色52吲哚D2(X
,(I)琼脂。该法的原理是α葡
释放糖苷配基52溴242氯2吲哚,该糖苷
2氯2吲哚,使菌落呈现特异性蓝绿。该改良法已被广泛应用,相对经典方法能缩短时间2天左右,且特异性高[9]。3.1.3 改良法:荧光选择性鉴别培养基法[10] 该方法也是利用α2葡萄糖苷酶活性的检测方法。在营养琼脂基础上添加
α242甲基2伞形酮2D2葡萄糖苷(α2MUG)。阪崎肠杆菌在该培
养基上形成黄色菌落,在紫外光照射下发生荧光。该法灵敏度和特异性都比较好,已在多个国家开展使用,均取得稳定可靠的结果。3.1.4 改良法:对硝基酚光电比色法[27] 利用阪崎肠杆菌αα的2葡萄糖苷酶活性,分解对硝基酚22D2葡萄糖苷底物,释放黄色的对硝基酚,在405nm波长下测定吸光度,根据吸光度的大小,确定样品中阪崎肠杆菌是否存在。方法是常规增菌,在VRBG或TSA平板上挑取可疑菌落,制备成一定浓度的菌悬液与底物混匀,37℃4h后进行比色测定。3.1.5 阳离子磁性珠快速捕获法[28] MULLANCE等设计了革兰阴性杆菌捕获系统,能快速富集阪崎肠杆菌。他将普通珠子经过顺磁化后,使其表面带有阳离子(正电荷),能极强地吸附带有阴离子(负电荷)的物质;革兰阴性杆菌表面的脂多糖就是带阴离子(负电荷)的物质,故阳离子磁性珠能捕获含有脂多糖的革兰氏阴性杆菌。MULLANCE将该系统设计成自动化,即将婴儿配方奶粉溶解后,通过管道输送至捕获器,反复与磁性珠接触,使阪崎等革兰阴性杆菌被吸附在磁性珠表面,然后在蛋白胨缓冲液中洗脱细菌;整个过程在6h内完成。然后将浓缩的菌液划线,接种在选择性显色培养基(DFI)或通过PCR分子生物学方法鉴定。使用该方法,最多在48h内鉴定出阪崎肠杆菌,比美国FDA经典方法缩短5天左右,并且灵敏度很高,可检出1~5CFU/500g奶粉。3.2 分子生物学方法
[29]
3.2.1 PCR方法 IVERSEN等利用16SDNA基因序列的PCR方法,对126株被API20E和ID32E自动化鉴定为阪崎肠杆菌,其中有几株是ATCC的标准菌株,进行了核苷序列分析。发现阪崎肠杆菌与柯氏枸橼酸杆菌最接近,有97.8%同源,而与阴沟肠杆菌只有97%同源;利用16SDNA核苷序列分析,可将126株阪崎肠杆菌进一步分为四个亚群:与标准菌株相比,有0.1%~1.2%序列不同的分为Ⅰ群,共有110株;有1.6%~1.9%序列不同分为Ⅱ群,共有9株;有97.5%~97.8%同源分为Ⅲ群,包括分类为Pyrinus肠杆菌、霍氏肠杆菌和柯氏枸橼酸杆菌,共有5株;第Ⅳ群仅2株,只有96.5%同源性。
[30]
LEHNER等则采用针对16SrRNA基因序列的PCR方法。他们对47株不同来源的阪崎肠杆菌和28株其他肠杆菌进行了分析,经与基因库标准菌株对比,47株阪崎肠杆菌有99.4%~100%同源性,28株非阪崎肠杆菌则全部阴性,特异性很强,灵敏度可达10pg。
[31]
MANOJ等设计了针对阪崎肠杆菌外膜蛋白A基因(OmpA)序列的PCR方法,所设计的产物能特异性地扩增阪
阪崎肠杆菌 阪崎肠杆菌研究进展_梁鹰
[2]FARMARJJⅢ,ASBARYMA,BRENNERDJ,etal.Enterobacter
sakazakii:anewspeciesof“Enterobacteria”isolatedfromclinicalspecimens[J].IntJSystBacteriol,1980,30:5692584.[3]URMENYIAM,WHITE2FRANKLINA.Neonataldeathfrompigmen2
tedcoliforminfection[J].Lancet,1961,1:3132315.
[4]JointFAO/WHOWorkshoponEnterobactersakazakiiandothermicro2
organismsinpowderinfantfomula,Geneva,225,February2004[EB/OL]..
[6]中国出入境检验检疫行业标准.SN/T163222005奶粉中阪崎肠杆菌检验方法,第1部分:分离与计数方法.2005.www.bzcbs.com/produce.
[7]NAZAROWEC2WHITEM,FARBERJM.Enteratactersakazakii:are2
view[J].IntJFoodMicrobiol,1997,34(2):1032113.[8]BREEUWERP,LARDEAUA,PETERZM,etal.Desicationandheat
toleranceofEnterobactorsakazakii[J].ApplMicrobiol,2003,95(5):9672973.[9]IVERSENC,DRUGGANP,FOSYTHES.Aseleetivedifferentialmedi2
umforEnterobactersakazakii,apreliminarystudy[J].IntJFoodMi2
ChineseJournalofMicroecology,Aug2008,Vol120No14
crobiol,2004,96(2):1332139.
[10]OHSW,KANGDH.Fluorogenicselectiveanddifferentialmedium
forisolationofEnterobactersakazakii[J].ApplEnvironMicrobiol,2004,70(9):569225694.
[11]MUYTJENSHL,vanderROS2vandeREPEJ,vanDRUTENHA.
EnzymaticprofilesofEnterobactersakazakiiandrelatedspecieswithspecialrefenencetothealpha2glucosidasereactionandreproducibilityofthetestsystem[J].JClinMicrobiol,1984,20(4):6842686.
[12]POSTUPAR,ALDOVAE.Enterobactorsakazakii:atween80esvase
positiverepresentativeofthegenusEntergbactorsakazakiiisolatedfrompowderedmilkspecimens[J].JHygEpidemiolMicrobiollmmunol,1984,28(4):4352440.
[13]LEHNERA,STEPHANR.Eicrobiologal,epidemiological,andfood
safetyaspectsofEnterobectersakazakii[J].JFoodProt,2004,67(12):285022857.
[14]PAGOTTOFJ,NAZAROWEC2WHITEMAWIDS,etal.Enter2
obacter:infectivityandponinvitroandinvivo[J].JProt,(3:2[15],,谢均宪.[J].中国21(4):J,2CARRILLOC,etal.Thepres2
powderedinfantformulamilkandinfluenceofen2sakazakiionbacterialtranslocationinthein2rat[J].FoodMicrobiol,2007,24(1):67274.[17]MANGEJP,STEPHANR,BORELN,etal.Adhesivepropertiesof
Enterobactersakazakiitohumanepithelialandbrainmicrovascularen2dothelialcells[J].BMCMicrobio,2006,6:58.[18]KIMH,RYUJH,BEUCHATLR.Attachmentofandbiofilmforma2
tionbyEnterobactersakazakiionstainlesssteelandenteralfeedingtubes[J].ApplEnvironMicrobiol,2006,72(9)584625856.[19]MUYTJENSH,ZANENHC,SONDERKAMPHJ,etal.Analysisof
eightcasesofneonatalmeningitisandsepsisduetoEnterobactersaka2zakii[J].JClinMicrobiol,1983,18(1):1152120.[20]BIERINGG,KARLSSONS,CLARKNC,etal.Threecasesofneo2
natalmeningitiscausedbyEnterobactersakazakiiinpowderedmilk[J].JClinMicrobiol,1989,27(9):205422056.
[21]BOWENAB,BRADENCR.InvasiveEnterobactersakazakiidisease
ininfants[J].EmergInfectDis,2006,12(8):118521189.
[22]MONROEPW,TIFTWL.BacteremiaassociatedwithEnterobacter
sakazakii(Yellow2pigmentedEnterobaterdoacae)[J].JClinMicrobi2al,1979,10(6):8502851.[23]ACKERJV,SMETFD,MUYLDERMANSG,etal.Outbreakofne2
crotizingenterocolitisassociatedwithEnterobactersakazakiiinpow2deredmilkformula[J].JClinMicrobiol,2001,39(1):2932297.
[24]周庭银,马子行.从三例患者重复分离出阪崎肠杆菌[J].临床检验杂志,1994,(12)增:76277.
[25]龚燕,顾学章.阪崎肠杆菌肺炎64例临床及药敏分析[J].上海医学,2005,28(12):104721048.[26]SEEKC,THANHA,TANGT.Enterobactersakazakiibacteremia
withmultiplesplenicabscessesina752year2oldwoman:acasereport[J].AgeAgeing,2007,36(5):5952596.[27]KANDHAIMC,REIJMW,VANPUYVELDEK,etal.Anewproto2
colforthedectionofEnteroberctersakazakiiappliedtoenvironmentalsamples[J].JFoodProt,2004,67(6):126721270.[28]MULLANENR,MURRAYJ,DRUDYD,etal.DetectionofEnter2
obactersakazakiiindriedinfantmilkformulabycationic2magnetic2
(boendcapture.[J].ApplEnvironMicrobiol,2006,729):63252
6530.[29]IVERSENC,WADDINGTENM,STEPHENLW,etal.Identification
andphylogenyofEnterobactersakazakiirelativetoenterobacterandcitrobacterspecies[J].JClinMicrobiol,2004,42(11):536825370.[30]LEHNERA,TASARAT,STEPHANR.16SrRNAgenebasedanaly2
sisofEnterobactersakazakiistrainsfromdifferentsourcesanddevelop2mentofaPCRassayforidentification[J].BMCMicrobiol,2004,4:43.
[31]NAIRMKM,VENKITANARAYANANKS.Cloningandsequencing
oftheompAgeneofEnterobactersakazakiianddevelopmentofanom2pA2TargetedPCRforrapiddetectionofEnterobactersakazakiiininfantformula[J].ApplEnvironMicrobiol,2006,72(4):253922546.
四 : 阪崎肠杆菌的菌落特征
阪崎肠杆菌 -菌落特征在胰蛋白胨琼脂(TSA)、脑心浸液琼脂(BHI)及血平板上经25~36℃培养24h后,形成1.5~2.5mm,黄色菌落,菌落形态有2种:一种为典型的光滑型菌落,极易被接种环移动,另一种为干燥或粘液样,周边呈放射状,不易被接种环移动,似橡胶状有弹性。后一种经传代后可转化为有光泽的菌落。
(www.61k.com) 本文标题:阪崎肠杆菌-阪崎肠杆菌:阪崎肠杆菌-概述,阪崎肠杆菌-发现过程61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1