一 : 分别分解高锰酸钾、氯酸钾(化学式KClO3)、过氧化氢(化学式H2O2)三种物质,都可以制得氧气。这
| 分别分解高锰酸钾、氯酸钾(化学式KClO3)、过氧化氢(化学式H2O2)三种物质,都可以制得氧气。这说明三种物质的组成中都含有 |
| [ ] |
| A.氧化物 B.氧元素 C.氧分子 D.氧气 |
| B |
考点:
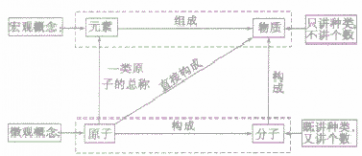
考点名称:元素的定义概念:元素是具有相同核电荷数(即核内质子数)的一类原子的总称。| 元素 | 原子 | |
| 概念 | 具有相同核电荷数〔即核内质子数)的一类原子的总称 | 化学变化中的最小粒子 |
| 区分 | 只讲种类,不讲个数 | 既讲种类,又讲个数 |
| 使用范围 | 用于描述物质的宏观组成 | 用于描述物质的微观构成 |
| 举例 | 水由氢元素和氧元素组成,或说水中含有氢元素和氧元素 | 每个水分子由两个氢原子和一个氧原子构成 |
| 联系 | 元素和原子是总体和个体的关系,原子是元素的个体,是构成并体现元素性质的最小微粒;元素是一类原子的总称一种元素可以包含几种原子 | |
二 : 烷基苯在高锰酸钾的作用下,侧链被氧化成羧基,例如化
| 烷基苯在高锰酸钾的作用下,侧链被氧化成羧基,例如 |
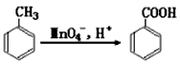 |
| 化合物A-E的转化关系如图1所示,已知:A是芳香化合物,只能生成3种一溴化合物,B有酸性,C是常用增塑剂,D是有机合成的重要中间体和常用化学试剂(D也可由其他原料催化氧化得到),E是一种常用的指示剂酚酞,结构如图2。 |
 |
| 写出A、B、C、D的结构简式: (1)A:______________。 (2)B:______________。 (3)C:______________。 (4)D:______________。 |
(1)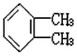 (2)  (3) 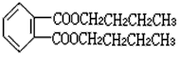 (4) 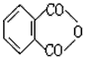 |
考点:
考点名称:有机物的推断有机物推断的一般方法: 的量,确定分子中不饱和键的类型及数目;由加成产物的结构,结合碳的四价确定不饱和键的位置。
的量,确定分子中不饱和键的类型及数目;由加成产物的结构,结合碳的四价确定不饱和键的位置。 根据反应现象推知官能团:
①能使溴水褪色,可推知该物质分子中可能含有碳碳双键、三键或醛基。
②能使酸性高锰酸钾溶液褪色,可推知该物质分子中可能含有碳碳双键、三键、醛基或为苯的同系物。
③遇三氯化铁溶液显紫色,可推知该物质分子含有酚羟基。
④遇浓硝酸变黄,可推知该物质是含有苯环结构的蛋白质。
⑤遇I2水变蓝,可推知该物质为淀粉。
⑥加入新制氢氧化铜悬浊液,加热,有红色沉淀生成;或加入银氨溶液有银镜生成,可推知该分子结构有-CHO即醛基。则该物质可能为醛类、甲酸和甲酸某酯。
⑦加入金属Na放出H2,可推知该物质分子结构中含有-OH或-COOH。
⑧加入NaHCO3溶液产生气体,可推知该物质分子结构中含有-COOH或-SO3H。
⑨加入溴水,出现白色沉淀,可推知该物质为苯酚或其衍生物。
根据物质的性质推断官能团:
能使溴水褪色的物质,含有C=C或C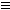 C或-CHO;能发生银镜反应的物质,含有-CHO;能与金属钠发生置换反应的物质,含有-OH、-COOH;能与碳酸钠作用的物质,含有羧基或酚羟基;能与碳酸氢钠反应的物质,含有羧基;能水解的物质,应为卤代烃和酯,其中能水解生成醇和羧酸的物质是酯。但如果只谈与氢氧化钠反应,则酚、羧酸、卤代烃、苯磺酸和酯都有可能。能在稀硫酸存在的条件下水解,则为酯、二糖或淀粉;但若是在较浓的硫酸存在的条件下水解,则为纤维素。
C或-CHO;能发生银镜反应的物质,含有-CHO;能与金属钠发生置换反应的物质,含有-OH、-COOH;能与碳酸钠作用的物质,含有羧基或酚羟基;能与碳酸氢钠反应的物质,含有羧基;能水解的物质,应为卤代烃和酯,其中能水解生成醇和羧酸的物质是酯。但如果只谈与氢氧化钠反应,则酚、羧酸、卤代烃、苯磺酸和酯都有可能。能在稀硫酸存在的条件下水解,则为酯、二糖或淀粉;但若是在较浓的硫酸存在的条件下水解,则为纤维素。
(4)根据特征数字推断官能团
①某有机物与醋酸反应,相对分子质量增加42,则分子中含有一个-OH;增加84,则含有两个-OH。缘由-OH转变为
-OOCCH3。
②某有机物在催化剂作用下被氧气氧化,若相对分子质量增加16,则表明有机物分子内有一个-CHO(变为-COOH);若增加32,则表明有机物分子内有两个-CHO(变为-COOH)。
③若有机物与Cl2反应,若有机物的相对分子质量增加71,则说明有机物分子内含有一个碳碳双键;若增加142,则说明有机物分子内含有二个碳碳双键或一个碳碳叁键。
根据反应产物推知官能团位置:
①若由醇氧化得醛或羧酸,可推知-OH一定连接在有2个氢原子的碳原子上,即存在-CH2OH;由醇氧化为酮,推知-OH一定连在有1个氢原子的碳原子上,即存在 ;
;
若醇不能在催化剂作用下被氧化,则-OH所连的碳原子上无氢原子。
②由消去反应的产物,可确定-OH或-X的位置
③由取代反应产物的种数,可确定碳链结构。如烷烃,已知其分子式和一氯代物的种数时,可推断其可能的结构。有时甚至可以在不知其分子式的情况下,判断其可能的结构简式。
④由加氢后碳链的结构,可确定原物质分子C=C或C C的位置。
C的位置。
根据反应产物推知官能团的个数:
①与银氨溶液反应,若1mol有机物生成2mol银,则该有机物分子中含有一个醛基;若生成4mol银,则含有二个醛基或该物质为甲醛。
②与金属钠反应,若1mol有机物生成0.5molH2,则其分子中含有一个活泼氢原子,或为一个醇羟基,或酚羟基,也可能为一个羧基。
③与碳酸钠反应,若1mol有机物生成0.5molCO2,则说明其分子中含有一个羧基。
④与碳酸氢钠反应,若1mol有机物生成1molCO2,则说明其分子中含有一个羧基。
根据反应条件推断反应类型:
①在NaOH水溶液中发生水解反应,则反应可能为卤代烃的水解反应或酯的水解反应。
②在氢氧化钠的醇溶液中,加热条件下发生反应,则一定是卤代烃发生了消去反应。
③在浓硫酸存在并加热至170℃时发生反应,则该反应为乙醇的消去反应。
④能与氢气在镍催化条件下起反应,则为烯、炔、苯及其同系物、醛的加成反应(或还原反应)。
⑤能在稀硫酸作用下发生反应,则为酯、二糖、淀粉等的水解反应。
⑥能与溴水反应,可能为烯烃、炔烃的加成反应。
根据反应类型推断官能团: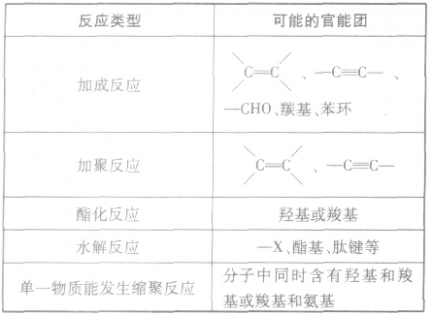
利用官能团的衍生关系进行衍变(从特定的转化关系上突破):
(1)
(2)芳香化合物之间的相互转化关系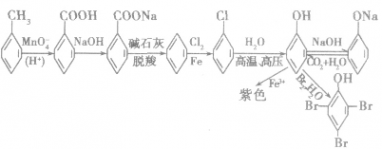
三 : 写出反应的化学方程式:加热高锰酸钾制取氧气____________.
| 写出反应的化学方程式:加热高锰酸钾制取氧气____________. |
2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
考点:
考点名称:化学反应方程式的书写化学方程式的书写原则遵循两个原则: 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 | 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。  CaO+ CO2↑
CaO+ CO2↑ CO2
CO2 2CuO
2CuO 四 : 写出反应的化学方程式:加热高锰酸钾制取氧气____________.
| 写出反应的化学方程式:加热高锰酸钾制取氧气____________. |
2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
考点:
考点名称:化学反应方程式的书写化学方程式的书写原则遵循两个原则: 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 | 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。  CaO+ CO2↑
CaO+ CO2↑ CO2
CO2 2CuO
2CuO 五 : 高锰酸钾制取氧气化学式
高锰酸钾这个词可能我们在日常生活中并不会经常见到,但是我们的生活中却会经常用到它,它常用作消毒剂、水净化剂、氧化剂、漂白剂、毒气吸收剂、二氧化碳精制剂等来使用,具有很多的功能,还能够从中获取我们生存所需的氧气。
一.高锰酸钾制取氧气化学式
KMnO4,高锰酸钾常温下即可与甘油等有机物反应甚至燃烧(但有时与甘油混合后反应极为缓慢,甚至感受不到温度的升高,其原因尚不明确);在酸性环境下氧化性更强,能氧化负价态的氯、溴、碘、硫等离子及二氧化硫等。与皮肤接触可腐蚀皮肤产生棕色染色,数日不褪;粉末散布于空气中有强烈刺激性,可使人连打喷嚏。尿液、二氧化硫等可使其褪色。与较活泼金属粉末混合后有强烈燃烧性,危险。该物质在加热时分解:
2KMnO4=△=K2MnO4+MnO2+O2↑
文字:高锰酸钾加热后生成锰酸钾和二氧化锰和氧气
高锰酸钾在酸性溶液中还原产物为二价锰离子
高锰酸钾在碱性溶液中还原产物一般为墨绿色的锰酸钾(K2MnO4)。
高锰酸钾在中性环境下还原产物为二氧化锰。
维生素C的水溶液能使高锰酸钾溶液褪色,并且维生素C溶液越浓,水溶液用量就越少。根据这一特性,就能够用高锰酸钾测定蔬菜或水果中的维生素含量。高锰酸钾造成的污渍可用还原性的草酸、维生素C等去除。强氧化剂,在酸性条件下氧化性更强,可以用做消毒剂和漂白剂,和强还原性物质反应会褪色,如SO2、不饱和烃
二.取氧气步骤
1.检查装置的气密性
用手紧握试管,观察水中的导管口有没有气泡冒出,如果有气泡冒出,说明装置不漏气(依据:用手紧握试管,试管内的气体受热膨胀,气体的体积增大,气压变大,如果不漏气,水中的导管口会有气泡冒出)。
2.装药品
先使试管倾斜,把盛有药品的药匙(或纸槽)送至试管底部,然后使试管直立起来。在试管口放一团棉花(目的:防止加热时高锰酸钾粉末进入导管),用带有导管的塞子塞紧瓶口,伸进试管内的导管不宜太长,稍伸出胶塞即可(目的:有利于气体的导出)。
3.固定仪器
把试管口略向下倾斜(目的:防止冷凝水回流到热的试管底部,炸裂试管)固定在铁架台上,铁夹应夹在距试管口约1/3处。
4.加热
先使酒精灯火焰在试管下方来回移动,让试管均匀受热,然后对高锰酸钾所在的部位加热。
5.收集
当气泡连续且比较均匀地放出时,再把导管口伸入盛满水的集气瓶里(原因:开始时水槽中导管末端有少量不连续的气泡冒出是受热膨胀的空气)。把集气瓶正放在桌子上(原因:相同条件下氧气的密度略大于空气的密度)。
6、验满
排水集气法:集气瓶口处有较大气泡冒出,则说明氧气收集满;向上排空气法:将带火星的木条放在集气瓶口附近,若复燃,则说明氧气收集满。(检验方法:将带火星的木条伸入集气瓶内,若复燃,则说明是氧气。)
7、先把导管移出水面,再熄灭酒精灯
目的:防止试管内气体冷却后压强减小,水槽中的水倒吸进热的试管中,使试管炸裂)。
三.制取氧气的问题
1.如何检验装置的气密性?
连接好装置,将导管放置在盛有水的水槽中,用手紧握试管,水中的导管口会有气泡冒出;松手后,有少量水会进入到导管或试管中。这说明装置的气密性良好。
2.为何用排水法或向上排空气法收集氧气?
氧气不易溶于水,且不与水反应,因此可用排水法收集氧气;相同情况下,氧气的密度比空气大,因此可用向上排空气法收集氧气。
3.为什么在试管口放一团棉花?为什么固体药品加热需要将试管口向下倾斜?为什么先预热,后固定加热?为什么要用外焰加热?
在试管口放一团棉花的原因是:防止加热时高锰酸钾粉末进入导管;固体药品加热需要将试管口向下倾斜的原因是:防止冷凝水回流到热的试管底部,炸裂试管;先预热,后固定加热的原因是:防止试管受热不均匀,炸裂试管;用外焰加热的原因是:酒精灯的外焰温度最高。
4.为什么导管口开始有气泡时,不宜立即收集?而当气泡连续且均匀冒出时,才能收集?
开始有气泡冒出时,是由于试管内空气受热膨胀,进入导管后排出的。而当气泡连续均匀放出时,说明试管内空气已基本排净,此时收集,可以收集到较为纯净的氧气。
利用高锰酸钾来获取氧气的事是大家众所周知的,在这里,小编就为大家详尽的介绍了利用高锰酸钾来获取氧气的化学式以及具体的操作步骤,相信你学会了这样的步骤,也可以自己来操作一下,看看能否利用高锰酸钾的化学式从试验中获取氧气。
本文标题:高锰酸钾制取氧气化学式-分别分解高锰酸钾、氯酸钾(化学式KClO3)、过氧化氢(化学式H2O2)三种物质,都可以制得氧气。这61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1