一 : 骨髓异常增生综合征是什么?
骨髓异常增生综合征是一组以难治性贫血及其他就是血细胞减少为特点系原因素质未明的细胞突变导致造血干细胞功能异常引起病态和无效造血的疾病骨髓表现为红细胞系粒细胞系和巨核细胞系不同程度的分化成熟障碍伴质和量的异常目前尚无有效的号费治疗措施部分病人各地在病程晚期转化为急性白血病(AL)
造血细胞的形态学异常 血象骨髓象均有异常改变
血象 红细胞白细胞血小板有一项或一项以上数量减少以贫血最为突出呈正细胞正色素性贫血血片中可出现巨大红细胞和有核红细胞各阶段幼稚粒细胞小巨核细胞及巨大畸形血小板
骨髓象 多数原因病人骨髓增生活一段跃显示系病态造血:①红系增生明显能力粒红比例倒置各阶段幼红细胞出现核浆发育不平衡呈巨幼样变可见双核多核分叶核及核畸形的幼红细胞胞浆着色不匀铁染色显示数量不一的环状铁粒幼红细胞②粒系部分太贵病人原始细胞增多但均<%各阶段可出现双核粒细胞中幼粒及晚幼粒细胞核浆发育不平衡胞浆着色不匀颗粒缺如减少或增多成熟中性粒细胞呈分叶过多或不分叶即出现类佩尔赫尔-希埃特二氏细胞畸形③巨核系出现原始幼稚及小巨核细胞巨核细胞可呈大单个核多圆核分叶核核畸形等异常可见体积增大和畸形的血小板
上述三系造血细胞的形态学异常也可见于周围血细胞
骨髓组织学改变 骨髓活检的组织学变化有一定诊断父母价值①未成熟粒细胞异位原始和早幼粒细胞个人正常时分布在骨小梁附近骨髓异常增生时成簇地移位于骨小梁间隙中此种移位和血及骨髓中的原始细胞数呈正相关移位明显不配者转为白血病的百分率高②原红细胞岛即原始或早幼红细胞聚集成岛状③巨核细胞大小不等核与浆比例扩大有核仁可见原始幼稚及小巨核细胞④半数以上病人痛苦网硬蛋白增多
造血细胞的功能异常 造血细胞功能障碍表现在博士铁利用障碍医者病人发生铁粒幼红细胞性贫血维生素B叶酸无法正常宝宝利用产生形态学类似于巨幼红细胞贫血的难治性贫血粒细胞杀菌吞噬能力个人减弱粘附及趋化性降低细胞动力学研究证实骨髓中S期(DNA合成期)细胞增加M期(有丝分裂期)细胞减少细胞周期时间时间延长提示细胞分裂分化及成熟障碍
MDS时骨髓增生旺盛而周围血细胞减少伴成熟细胞的功能障碍因此主要胃癌病理为无效造血
染色体和造血干细胞体外培养异常 MDS有染色体畸变者占半数以上其表现多种多样无规律性至今尚未发现特异的标记染色体;多数有用病人造血干细胞的体外培养可见粒巨噬细胞集落形成单位(GM-CFU)红细胞爆发形成单位(BFU-E)红细胞集落形成单位(CFU-E)粒嗜酸巨噬巨核细胞集落形成单位(GEMM-CFU)巨核细胞集落形成单位(M-CFU)数量均不想明显减少甚至缺如
骨髓异常增生综合征的分型:
据年FAB协作组主任建议MDS分为型:
难治性贫血(RA) 以贫血为主要信赖症状很高白细胞减少者常伴发性格各种感染血小板减少者有出血倾向血象中以红细胞减少为主可伴白细胞和(或)血小板降低网织红细胞不清正常或减少原始细胞<%骨髓有上述系或系细胞病态造血名医现象原始细胞<%
难治性贫血伴铁粒幼红细胞(RAS) 具备难治性贫血的特点骨髓中环状铁粒幼红细胞≥%
难治性贫血伴原始细胞过多(RAEB) 具备RA的特点原始细胞在周围血为~%在骨髓中占~%
转化中的难治性贫血伴原始细胞过多(RAEB-T) 具备RA的特点原始细胞在血片中>%在骨髓中占~%部分原始细胞可见奥尔氏棒状小体
好转慢性粒单核细胞性白血病(CMML) 除具有RA的特点外血象中成熟单核细胞>/L原始细胞<%骨髓同RAEB但成熟单核细胞增多原始单核细胞<%
骨髓异常增生综合征的正确诊断标准:
血象一般检查一系或一系以上血细胞减少出现有核红细胞及幼稚粒细胞常有各系细胞病态造血的形态学异常;骨髓象增生活帮助跃有两系细胞病态造血的形态学异常出现少量原始细胞;除外有病其他引起病态造血的疾病及不典型急性白血病
骨髓异常增生综合征的鉴别诊断信心:
应与以下疾病加以鉴别
巨幼细胞性贫血其血象骨髓象和RA颇为相似血清维生素B或叶酸副作用水平明显亲自降低及试验性你们治疗有效为鉴别要点(见巨幼细胞性贫血)
不典型再生障碍性贫血(AA) 部分AA骨髓增有病生活跃但无病态造血而非造血细胞常增多藉此可和RA区别且周围血中不应出现幼稚细胞
阵发性睡眠性血红蛋白尿(PNH) 不发作组PNH呈全血细胞减少血片中可见核红细胞骨髓红系增生好些明显易与RA混淆根据无病态造血酸化血清试验(哈姆斯氏试验)糖水试验蛇毒溶血试验及尿潜血含铁血黄素试验阳性可资鉴别
红白血病(M) 当骨髓红系>%时难与RAEB或RAEB-T鉴别应单独进行非红系细胞计数分类如原始细胞≥%则为M<%为MDS
低原始细胞性急性白血病 骨髓原始细胞较典型急性白血病(AL)外地明显降低仅占%左右临床和RAEB-T不易区分RAEB-T绝大多数在短期内转化为AL因此有人认为 RAEB-T基本上已处于AL的边缘不应归属于MDS
此外太差慢性粒单核细胞性白血病(CMML)已是一种白血病FAB协作组也给予白血病命名因此不少人认为应将CMML划归白血病范畴
骨髓异常增生综合征的治疗加号:
MDS病因女儿至今未明尚无副作用满意的加队治疗措施铁剂维生素BB及叶酸等抗贫血药物早点已证实无效雄激素仅对部分RARAS患者疲劳有提高血红蛋白的作用领导肾上腺皮质激素对有化验明显出血倾向者有一定止血效果难受维甲酸-二羟维生素D等细胞诱导分化高超药物的为了疗效尚有争论RAEBRAEB-TCMML应用小剂量阿糖胞苷三尖杉酯碱等的去年效果评价方案不一且评论暂时有效者多伴骨髓抑制因此仍可能中药为细胞毒有限作用几个试用强烈治病联合化学治疗多说的不愧报告其结果女儿人工也不因为满意异体骨髓花钱移植搭理治疗MDS已有成功周六的病例报道
二 : 骨髓增生异常综合征
中外健康文摘2010年;7,qlq7譬第21期w。rId
Health
Diges‘MedicⅢ。Perlo。die,alq:≈搋,粒舰"、;讯”n#‰,,“、x%%,、%,,帮。≈黼嘎∞j论
著
6.颜面手及其它功能部位深度烧伤刨面,应在休克期顺利度过以后,病情稳定的状态下,尽可能采取早期切痂植皮术。大面积Ⅲ度烧伤的小儿,更应早期切痂植皮。在手术过程中,必须注意呼吸循环功能的稳定,尽可能防止出血过多,缩短手术时间,保证输液与输血。
7、小儿皮炎薄嫩对疼痛刺激耐受性差清刨时要轻柔,有耐心把创面刺激降低到最低限度。
=.小儿烧伤手术的麻醉用药特点
麻醉药选择的原则是安全、止痛完善、生理干扰小、清醒迅速、术后反应少,对生理功能无严重影响,患儿易于接受、无痛苦记忆,操作要尽可能简便。多数情况下不需要肌松。目前还没有最佳的烧伤麻醉药。优选快速代谢的麻醉药,患儿能够尽快苏醒、活动和进食。
烧伤病儿手术大多数是在全身麻醉下完成,并根据具体情况决定是否行气管内插管以保证呼吸道通畅。麻醉方法包括全凭静脉、静吸复合麻醉、局麻或神经阻滞复合全麻等。
1.麻醉诱导静脉诱导较简便,如静脉通道不易建立,可以使用吸入诱导。
2.麻醉维持可采用吸人麻醉、全凭静脉麻醉、静吸复合麻醉。(三)其他麻醉方法
烧伤病儿手术较少应用局部麻醉和区域阻滞麻醉。对上肢或下肢广泛烧伤,如患儿合作或配合基础麻醉,可应用臂丛阻滞、脊麻或硬膜外麻醉。如上肢手术可采用臂神经丛阻滞麻醉,下肢手术可选用连续硬膜外麻醉,对全身影响较小。
(四)特殊烧伤病人的麻醉
大面积严重烧伤,特别是伴有头.面部、呼吸道等特殊部位的烧伤,麻醉处理十分困难,此类病人常伴有低血容量.严重贫血,低蛋白血症、水电解质与酸碱失衡,难以维持气道通畅。对于这些患儿,术前不仅要纠正贫血和内环境紊乱,以提高耐受麻醉的能力.并充分评估气道情况,确保气道通畅。除此之外,还应注意以下问题:
1.术前应充分止痛,缓解患儿疼痛,获得息儿配合。2.麻醉前必须对呼吸道情况及呼吸功能进行较全面了解,对面颈部极度肿胀病人.为确保气道通畅,术前可行气管造口术。
3.对肢体烧伤无法测量血压,脉率的病人,应借助观察尿量,CVP,心率、ECG等变化,了解循环情况。
4.大面积烧伤后,患儿常需多次手术和麻醉,每次手术不仅出血多,时间长,机体消耗严重,患儿常难以承受深麻醉对呼吸、循环等的抑制作用。
5.大面积烧伤后,常无法行静脉穿刺,外套管针的广泛应用有利于实施液体治疗及静脉给药。
参考文献
【1】耿荣.小儿全身炎症反应综合征.1997(05).
【2】郑庆亦,车梅发,叶国安.小儿重度烧伤休克期输全血的临床观察.199l(01).
f3】刘宗民,贺柏林,宋运琴.阈下剂量氯胺酮与异丙酚并用的临床研究.1995(09).
【4】王玲,唐时荣,邹清远.微泵静注异丙酚一氯胺酮复合麻醉用于烧伤病人【期刊论文】一中华麻醉学杂志.2000(06).
骨髓增生异常综合征
许晓舜
【中图分类号】R551.3
【摘要1
日的
(黑龙江省八五七农场职工医院
【文献标识码】A
158322)
I文章编号】1672--5085(2010)21—0091—02
对78例MDS血象、骨髓象、形态学及临床资料进行了回顾性
提高诊断骨髓增生异常综合征(MDs)的水平。方法
分析。结果78例外周血减少36例(46%),二系减少I8例(23%),分类可见幼红细胞34例(44%).幼粒25例(32%),贫血75例(97%).中、重度贫血62例(79%),表现为大细胞正细胞贫血异常54例(69%)。1o例难治性贫血患者病态造血不明显(12.8%)。结论MDS临床表现不典型,血液学改变繁杂.缺乏特异性。由于MDS这些特点.使其诊断白血病尤其显得困难,特别是形态学改变不明显时。
【关键词】骨髓增生综合征
骨髓增生异常综合征是一组克隆性造血干细胞疾病。特点是髓系中一系或多系发育异常和无效造血,表现为两种血细胞减少或全血细胞减少。尽管MDS以形态学分类时间不长,但描述该病已超过70年。
一,临床表现
MDS的临床症状和体征与外周血细胞减少有关,但缺乏特异性,许多患者可无明显自觉症状,因偶然的常规实验室筛检而明确诊断。部分患者有乏力、虚弱,运动不能、心绞痛、头晕、感染和出血。尽管MDS高感染率与中性粒细胞减少有密切关系,粒细胞功能包括趋化和杀伤作用受损也是高感染率发生的重耍因素。主要为细菌感染,感染可能隐蔽,抗生素不敏感且起效慢,是MDS患者死亡的主要原因。在没有全身性免疫抑制剂应用的情况下,真菌、病毒和分枝杆菌的感染罕见。
MDS的皮肤表现少见,但MDS合并Sweet综合征或急性热病性嗜中性粒细胞性皮肤病常预示向急性白血病转化。细胞因子如LL-6和粒细胞集落刺激因子(G-CSF)导致的自分泌和旁分泌与其有关,绿色瘤也可能预示疾病进展。
60%MDS患者体检可发现苍白,26%可有瘀点、瘀血,很
少有肝、脾和淋巴结的肿大。
=.低危治疗
目前低危患者不推荐强烈化疗或干细胞移植。症状性贫血:1.非低增生性骨髓
(1)不适宜应用免疫抑制剂者可考虑应用
1)RA/RAEB(不适宜化疗或干细胞移植)+血清EPO<200U/L,少/无需输血(每月<2UX考虑EPO10000U/d实验性治疗6周,如无反应每日加用G-CSF治疗或者将EPO剂量加倍,或者既加G-CSF又将EPO加量继续用6周。G-CSF剂量应从75“
g-÷150
u
g一300
u
g每周递增使白细胞维持在6~10
X
109/L
有反应的患者一旦其治疗反应达到最高水平即可将G-CSF减至1周3次l而EPO每4周减1次至每周5、4、3天直至最低维持荆量。
2)MRS+血清EPO<500U/L,少/无需输血(每月输血量<2UX考虑EPO+G-CSF(剂量同M/MEB)实验性治疗6~12周,如无反应可将EPO逐渐加量继续治疗6周。
3)其他:高水平血清EPO+/-大量输血。(2)如合适可考虑用免疫抑翩剂抗淋巴细胞球蛋白。
一91—
论
著。《群《㈣。。澎,缈柳。/蜷,。。。,∥,。。镕繇。,。。∞g,¥舻。。妻,健康事擅2~01,o予7月第7卷第21期,y。’Id熙a,l‘。h
(3)支持治疗
贫血的治疗:任何有症状的贫血患者都应考虑红细胞输注,
Dig。奠M。4‘cal,Pe一。6‘。丑l
平Iv)和达那唑(等级B,水平Ⅱb)偶尔有用,但不常规推荐。
4)感染的治疗:①预防,没有已发表的数据支持常规使用抗生素或抗真菌药来预防中性粒细胞减少的MDS患者发生感染。严重中性粒细胞减少的患者可考虑使用预防性低剂量>l患者一样静脉用抗生素。
2.低增生性骨髓考虑用免疫抑制剂抗淋巴细胞球蛋白(证据等级B,水平Ⅱbl用于非强烈化疗的药物:没有充分证据建议常规使用低剂量化疗如阿糖胞苷、马法兰等,尚无证据表明生存率或生活质量能从低剂量化疗中受益。
参考文献
【l】廖清奎.小儿血液病基础与临床【M】.北京:人民卫生出版社,2001:58l一588.
【2】王吉耀.内科学【M】.北京:人民卫生出版社。2005:
740-744.
X
而不应限定输血的最低血红蛋白浓度指征。只有一些患者如纯铁粒幼细胞性贫血或5q-综合征患者能长期输注红细胞,其他多数患者接受59铁(相当于输注25U红细胞)就应考虑去铁治疗(证据等级B。水平Ⅲ)。去铁胺每周5~7天,每隔12d,时输注20-40rag/l(g。在去铁胺治疗前必须进行听力及视力检测。治疗目标是控制铁蛋白浓度降至1000
I,t
l&/h
⑦治疗,MDS患者由于缺乏粒细胞发生脓毒症与其他粒细胞缺乏
g/L,如果铁蛋白浓度降至2000
pg/L,
应减少去铁胺用量,不超过25mg/kg。去铁胺治疗1个月后,应开始补充维生素C0.1~0.29/d,开始输注时即服用维生素C。至少每年复查1次听力和视力,如果不能耐受输注,可考虑2次/d皮下注射去铁胺。
2)免疫抑制治疗;现有资料支持至少可在低增生MDS患者进行免疫抑制治疗(马抗人淋巴细胞免疫球蛋白、环孢素A)(试验证据等级B,水平Ⅱb)。
一些治疗价值有限。并不常规推荐的药物。
3)血小板减少的治疗:输注血小板、抗纤溶药物(等级C,水
【3】任路英,乔桂芳.低增生型骨髓增生异常综合症的临床分析【J】.实用医技杂志,2001。8(4):258.
唑来膦酸联合放疗治疗恶性肿瘤骨转移临床观察
汪质良.(湖北省枣阳市一医院肿瘤科441200)
【中图分类号】R453
【关键词】唑来膦酸恶性肿瘤
【文献标识码】A
【文章编号】1672-5085(2010)21-0092-02
骨转移放疗化疗
止吐等治疗,3周连续重复使用3-5次,化疗组在化疗的当天给予唑来膦酸4mg溶于100ml生理盐水中静注,每4周为一周期,连续3-4周期,疼痛剧烈者,按照三阶梯止痛治疗原则使用止痛药物。
1.3观察指标
疼痛程度:采用视觉模拟评分法(VAS)对疼痛进行评分,测定疼痛强度。采用O一10数字疼痛强度分级法,由患者口述医生记录,0为无痛,1-3为轻度疼痛,4-6为中度疼痛,7一10为重度疼痛。本组病例均有骨痛,其中轻度12例,中度25例,重度38例。
体力状况ECOG评分:0分,无症状。活动没有影响,1分,有症状,但几乎完全可自由活动;2分,有时卧床,但白天卧床时
唑来膦酸是一种高效、含氨基的第三代双膦酸盐类药物,是目前公认治疗骨转移的有效药,能明显缓解患者疼痛,改善患者生活质量,防止或减少骨相关事件发生,不良反应少。自2007年
6月一2009年12月,我科应用唑来膦酸联合放疗治疗骨转移患者,现总结如下:
1.材料与方法
1.1临床资料:全组75例患都均为初发骨转移患者,75例骨转移疼痛患者均有原发肿瘤病理诊断,经ECT、MI或CT、X线诊断等检查进一步证实有骨转移,其中男42例,女33例,年龄在30_78岁,预计生存期>3个月,血常规、心、肝,肾功能无明显异常无化疗禁忌,多发骨转移患者选取疼痛剧烈的部分进行放疗,见表l
表l
75例恶性肿瘤患者病种分类和骨转移情况例
间不超过50‰3分,需要卧床,卧床时间白天超过50%;4分卧
床不起,本组病例活动能力0分30例,1分12例,2分18例,3分10例,4分5例。
不良反应:观察治疗期间患者有无发生恶心、呕吐、肌肉关节疼痛、疲乏、低钙血症、肾功能损伤及骨相关事件等不良反应。
1.4疗效评价标准
全组患者均在使用唑来膦酸3个周期后评价疗效
止痛:(1)完全缓解(CR),治疗后完全无痛;(2)部分缓解(PR)疼痛较治疗前明显减轻;(3)无效(NR)疼痛无减轻或加重。
体力状况ECOG评分:1)显效:活动能力改善≥2分;2)有效:活动能力改善1分;3)无效:活动能力未提高或弱。
2.结果
65例患者采用唑来膦酸联合局部放射治疗(放疗组),同期10例采用唑来膦酸联合化疗(化疗组)
1.2治疗方法
放疗组:采用外照射,北京医疗器械研究所直线加速器x一6my针对骨转移疼痛剧烈部位进行姑息性放疗,65例中病灶3Gy/次,5次/周,总剂量30Gy,放疗开始当天给予唑来膦酸4mg溶于100ml生理盐水中,静脉输注至少15分钟,并给予水化一92一
2.1镇痛及活动能力评价。(表2)表2放疗组和化疗组效能比较例%
放疗组与化疗组止痛有效率为95.8%和80%.有显著性差异(P<0.05),其中45例治疗使用止痛药物者,治疗后33例(73%)
三 : 骨髓增生异常综合征:骨髓增生异常综合征-病症简介,骨髓增生异常综合征
德胜门中医院血液科指出骨髓增生异常综合征是一组起源于造血髓系定向干细胞或多能干细胞的异质性克隆性疾患,主要特征是无效造血和高危演变为急性髓系白血病,临床表现为造血细胞在质和量上出现不同程度的异常变化。其具体临床表现为贫血,可伴有感染或出血,部分病人可无症状。部分患者可有肝,脾,淋巴结轻度肿大,少数患者可有胸骨压痛,肋骨或四肢关节痛。多数MDS病例以进行性的骨髓衰竭为特征,并最终都会发展成为AML,但是不同亚型转白率也不同,某些患者的生物学特征是相对惰性的,病程较长,转白率很低。在MDS定义明确后,诊断和分型中主要难点在那些外周血和骨髓原始细胞不增多病例上,尤其当病态造血不显著时,不能获得足够细胞分析可能的疾病过程。
骨髓异常增生综合征_骨髓增生异常综合征 -病症简单介绍
骨髓增生异常综合征(myelodysplasticsyndrome,MDS)是一组起源于造血髓系定向干细胞或多能干细胞的异质性克隆性疾患,其基本病变是克隆性造血干、祖细胞发育异常(dysplasia),导致无效造血以及恶性转化危险性增高,主要特征是无效造血和高危演变为急性髓系白血病,临床表现为造血细胞在质和量上出现不同程度的异常变化,MDS发病率约10/10万~12/10万人口,多累及中老年人,五十岁以上的病例占50%~70%,男女之比为2:1。MDS30%~60%转化为白血病,其死亡原因除白血病之外,多数由于感染、出血,尤其是颅内出血。
骨髓异常增生综合征_骨髓增生异常综合征 -疾病原因
发病原因
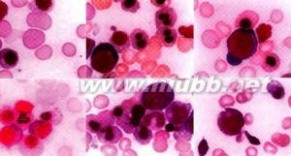
发病机制
MDS患者在致病因素作用下,引起患者造血干细胞损伤,用G6PD同工酶类型,X染色体伴限制性长度片段多态性甲基化,X染色体失活分析等方法已确定大部分MDS是病变发生在造血干细胞水平的克罗恩病,因而不但髓系,红系,巨核系细胞受累,淋巴细胞系亦受影响,导致T,B细胞数量和功能异常,临床表现为免疫缺陷或自身免疫性疾病,但在部分患者中其发病可仅局限在粒,红,巨核,巨噬祖细胞水平,仅有粒,红,巨核,巨噬细胞等受累而无淋巴细胞受累。骨髓异常增生综合征_骨髓增生异常综合征 -症状表现
多见贫血
骨髓增生异常综合症的临床表现无特殊性,此病患者通常起病缓慢,少数患者具有起病急剧的特点,一般从发病开始转化为白血病,此病患者在一年之内约有50%以上会转化为白血病,其中有贫血患者占90%,此类型患者就会有面色苍白、乏力、活动后心悸、气短等特点;当老年人出现贫血后会使原有的慢性心、肺疾病加重,此时出现发热的患者会占50%,其中原因不明性发热占10%~15%,此时患者会表现为反复发生的感染及发热,其中感染部位会以呼吸道、肛门周围和泌尿系最多。肢体部位出血
人们能够提前知晓骨髓增生异常综合症病人的症状表现,就会在自身有很多部位出血的情况及时来医院检查治疗,目前此病导致人们出血的患者就占20%,其中常见的出血部位包括呼吸道及消化道,有些患者也会有颅内出血,早期的出血症状较轻,大多是皮肤粘膜出血、牙龈出血或鼻衄;而女性患者就会有月经过多等表现,一旦病情到了晚期患者就会有出血趋势加重,而脑出血成为患者死亡的主要原因之一。脾、肝肿大
提醒大家脾肝肿大几乎是每位骨髓增生异常综合症患者都会出现的症状,病人会偶尔发现左上腹有一肿块,有人认为脾大程度与病程有关,脾肋下每1CM代表一年病程;而且由于脾大,患者经常有腹部饱满或沉重压迫的感觉,对脾触之坚实,一般无压痛;但如脾增大太快,人们就会因脾局部梗死而发生局部疼痛,甚至可以听到摩擦音。容易感染
人们得上骨髓增生异常综合症之后会因粒细胞减少和功能异常导致感染发生,病情初期比较稳定,患者多无严重的感染与发热,后期就比较容易合并感染;而且由于免疫力低下就会容引起潜在性脓疡以及化脓性关节炎、结核、绿脓杆菌性结膜炎、坏疽等不常见的感染;而且霉菌感染在后期较普遍,败血症也会成为疾病终末期的合并症和主要的死亡原因。骨髓异常增生综合征_骨髓增生异常综合征 -实验室检查
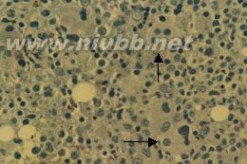
二、骨髓象
大多数患者骨髓增生明显或极度活跃,少数增生正常或减低。细胞形态异常反映了MDS的病态造血。红系各阶段幼稚细胞常伴类巨幼样变,核浆成熟失衡,红细胞体积大或呈卵园形,有嗜碱点彩、核碎裂和Howell-Jolly小体。RA-S能检出环形铁粒幼细胞。粒系在RAEB和RAEB-T均可见原始细胞比例高于正常。粒细胞浆内颗粒粗大或减少,核分叶过多或过少,出现Pelger-Hu?t 畸形。部分胞浆内出现Auer小体。巨核细胞在数和质方面均可有异常,多数巨核细胞增多。检出小巨核细胞是MDS的支持诊断指标之一。血小板体积大,颗粒少。
骨髓活检在MDS已广泛应用,不仅提供诊断依据,还有助于预测预后。骨髓病理切片中各系病态造血更加明显,特别是粒系。若发现3~五个以上原粒与早粒聚集成簇,位于小梁间区或小梁旁区,即所谓“幼稚前体细胞异常定位”(abnormal localization of immature precursor,ALIP),是MDS骨髓组织的病理学特征。凡ALIP阳性者,其向急性白血病转化可能性大,早期死亡率高。反之,则预后较好。
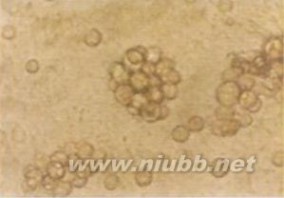
三、细胞遗传学研究
MDS是1种多能造血干细胞水平上突变的获得性克隆性疾病。过去,采用标准的染色体技术,31~49%原发性MDS患者中发现有某种染色体缺陷。近年,随着染色体技术的改进,异常克隆的检出率显著提高。特异性染色体改变有-7/del7q,+8,-5/del5q,和累及第5、7和20号染色体的复合染色体异常。非特异性染色体改变,如环形染色体、双着丝点染色体及染色体断裂等。染色体的检查对预测预后具有一定价值,骨髓中有细胞遗传学异常克隆的患者,其转化为急性白血病的可能性大得多,特别是-7/del7q和复合缺陷者,约72%转化为急性白血病,中数生存期短,预后差。
骨髓异常增生综合征_骨髓增生异常综合征 -诊断
1986年全国关于MDS的讨论会提出下列诊断标准:二、环形铁粒细胞性难治性贫血(RAS):
骨髓中环形铁粒幼细胞数为骨髓所有有核细胞的15%以上,其他同RA。
三、难治性贫血伴有原始细胞增多(RAEB)
血象:2系或全血细胞减少,多见粒系病态造血现象,原始细胞<5%。
骨髓:增生明显活跃、粒系及红系都增生。3系都有病态造血现象,原始细胞Ⅰ型+Ⅱ型为5%~20%。
四、慢性粒,单核细胞白血病(C美眉L)
血象:单核细胞绝对值>1×109/L。粒细胞也增加并有颗粒减少或Pelger-Huet异常。原始细胞<5%。
骨髓:同RAEB,原始细胞5%~20%。
五、转变中的RAEB(RAEB-T):血象及骨髓似RAEB,但具有下述3种情况的任1种:①血中原始细胞75%;②骨髓中原始细胞20~30%;③幼稚细胞有Auer小体。
六、了解临床伤人病史,包括药物最后和化学试剂的接触史很重要,鉴别骨髓增生异常时尤其是原始细胞不高的病例,要考虑非克隆性疾病,若诊断困难可在几个月后再行骨髓及细胞遗传学检查。
骨髓异常增生综合征_骨髓增生异常综合征 -治疗
支持治疗
当患者有明显贫血或伴心、肺疾患时,可输红细胞。RA和RA-S常因反复输血造成铁负荷增加。在有出血和感染时,可输入血小板和应用抗生素。预防性输注粒细胞和血小板对MDS患者无明确疗效。维生素治疗
部分RA-S对维生素B6治疗有效,200~500mg/日静滴,可使网织红细胞升高,输血量减少。肾上腺皮质激素
约10~15%MDS患者,应用肾上腺皮质激素治疗后,外周血细胞计数明显上升,但皮质激素治疗带来的易感染,血糖升高等副作用不容忽视。分化诱导剂
MDS患者恶性克隆中的某些细胞仍保留分化潜能,一些药物能诱导瘤细胞分化。目前常用的有1,25双羟维生素D3,2μg/d口服,用药至少12周。或用维生素D330~60万单位肌注,每日一次,8~28周。在用药中部分患者血象改善。该类药物可引起威胁生命的严重高血钙,故应严密监测血钙变化。13-顺式维甲酸在体外培养中有诱导分化作用,但临床应用不理想,国内多采用全反式维甲酸20mg每日三次口服。小剂量阿糖胞苷对髓性白血病有分化诱导作用,目前已用于MDS,特别是RAEB和RAEB-T,缓解率约30%,10~20mg/m2/d皮下注射,7~21天。但小剂量阿糖胞苷对骨髓的抑制作用仍不能忽视,约15%患者死亡与药物相关。雄激素
炔睾醇(danazol)是目前最常用的男性激素,600~800mgd,持续2~4月,但无确切疗效。有报道认为男性激素有加速向急性白血病转化的可能。联合化疗
就多数MDS而言,常规的抗白血病治疗无益。MDS对化疗耐受性低,治疗疗效差,即使获得缓解,缓解期也短。若病人年龄小于五十岁,处于RAEB-T临床状态好,可酌情用常规化疗。骨髓移植
当年龄小于五十岁,并处于RAEB或RAEB-T,有HLA同型供者,医疗条件允许,可考虑进行同种异体骨髓移植。骨髓异常增生综合征_骨髓增生异常综合征 -预后
MDS是1种异质性疾病,各型间生存期差异较大。RA和RA-S患者生存期常>5年,C美眉L、RAEB和RAEB-T患者中数生存期常<1年。感染、出血及向AML转化为主要死亡原因。
骨髓异常增生综合征_骨髓增生异常综合征 -生活调理

骨髓异常增生综合征_词条认领机构-求医网骨髓增生异常综合征专题

求医网(www.qiuyi.cn)创立于2000年,是北京时代网创科技发展有限公司核心平台,我们力求打造中国最专业的医疗网站。求医网正在努力为患者提供方便、快捷和专业的在线咨询服务,同时建立海量信息库为患者提供最全面的医疗信息资讯……详细 >>
本词条全部内容由词条认领机构及智愿者共同编辑,互动百科权威评审。
本文标题:骨髓增生异常综合征-骨髓异常增生综合征是什么?61阅读| 精彩专题| 最新文章| 热门文章| 苏ICP备13036349号-1